Bài viết của Thạc sĩ, Bác sĩ Mai Viễn Phương - Khoa Khám bệnh & Nội khoa - Bệnh viện Đa khoa Quốc tế Vinmec Central Park
Tyrosine kinase thụ thể RON (RTK; còn được gọi là MST1R) được xác định lần đầu tiên vào năm 1993 trong thư viện cDNA từ các tế bào biểu mô của người. RON thuộc họ proto-oncogenes c-MET. Họ RTK này chỉ có hai thành viên, RON và Met, chỉ có 34% tương đồng tổng thể; tuy nhiên, vùng tyrosine kinase của các thụ thể khá giống nhau ở mức tương đồng 80%.
Năm 1994, một cDNA của chuột được nhân bản mã hóa một chất tương đồng của RON, được gọi là thụ thể tyrosine kinase có nguồn gốc từ tế bào gốc. RON nằm ở nhiễm sắc thể 3p21 của con người và gen này cho thấy mức độ bảo tồn cao ở các loài khác nhau, bao gồm xenopus, cá ngựa vằn, gà, mèo, người và chuột. Ban đầu thụ thể RON được tổng hợp dưới dạng tiền chất chuỗi đơn không hoạt động về mặt sinh học (pro-RON), sau đó được phân cắt thành chuỗi β 145 kDa và chuỗi alpha ngoại bào 35 kDa, được liên kết bằng liên kết disulfide, tạo thành thụ thể trưởng thành.
1. Thụ thể RON và protein kích thích đại thực
Năm 1994, phối tử sinh lý của RON được xác định là protein kích thích đại thực bào (MSP) [còn gọi là protein giống yếu tố tăng trưởng tế bào gan (HGF)], thiết lập hệ thống tín hiệu protein kích thích đại thực bào -RON. Protein kích thích đại thực bào là một thành viên của họ protein kringle liên quan đến plasminogen. Gen protein kích thích đại thực bào của con người cũng nằm ở nhiễm sắc thể 3p21 và được bảo tồn về mặt tiến hóa ở các loài khác nhau, tương tự như RON. Nguồn chính của protein kích thích đại thực bào là tế bào gan và protein kích thích đại thực bào lưu thông trong máu dưới dạng pro-protein kích thích đại thực bào, là một tiền chất chuỗi đơn không hoạt động về mặt sinh học. Sau quá trình chuyển đổi phân giải protein tiếp theo, protein kích thích đại thực bào trưởng thành hoạt động bao gồm tiểu đơn vị alpha liên kết với disulfide và chuỗi β. Vị trí liên kết ái lực cao của thụ thể RON nằm trong chuỗi β và hoạt động của RON được điều chỉnh bởi chuỗi alpha. Sự gắn kết của protein kích thích đại thực bào với RON gây ra sự đồng phân hóa RON, kích hoạt nhiều con đường tín hiệu xuôi dòng, dẫn đến sự phát triển, tồn tại và xâm lấn của tế bào qua trung gian RON
2. Sự kích hoạt RON không bình thường trong các loại khối u khác nhau
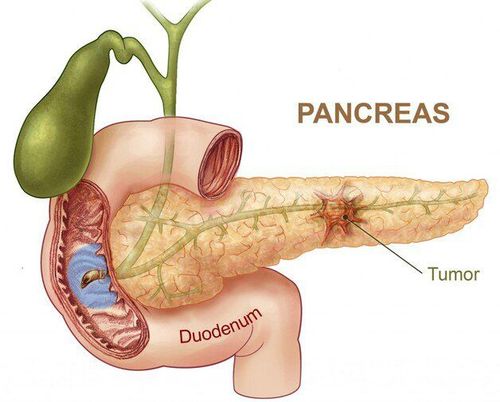
Trong hai thập kỷ gần đây, nhiều nghiên cứu đã tập trung vào vai trò gây khối u và điều trị của tín hiệu RON. Mặc dù có rất ít nghiên cứu liên quan đến những thay đổi liên quan đến bệnh lý trong biểu hiện protein kích thích đại thực bào, nhiều nghiên cứu liên quan đến sự kích hoạt RON không bình thường trong các loại khối u khác nhau đã được công bố, bao gồm biểu hiện quá mức của protein RON, thế hệ biến thể gây ung thư, và kích hoạt liên tục các con đường tín hiệu xuôi dòng. Ngoài ra, sự tiến triển của khối u và bệnh ác tính có liên quan đến nhiễu xuyên âm chức năng giữa các protein truyền tín hiệu và RON. Trong ứng dụng lâm sàng, tăng biểu hiện RON có thể được sử dụng để đánh giá tiên lượng khả năng sống sót của bệnh nhân và tiến triển của bệnh. Ung thư gan mật và ung thư tụy (HBP) có kết quả xấu, với tỷ lệ tử vong do ung thư cao vì tỷ lệ tái phát, di căn và xâm lấn cao, và không nhạy cảm với hóa trị liệu. Phẫu thuật cắt bỏ hoàn toàn vẫn là phương pháp điều trị hiệu quả nhất đối với ung thư HBP. Trong số các bệnh ung thư này, tỷ lệ sống sót sau 5 năm của ung thư gan là khoảng 30%, trong khi ung thư đường mật và ung thư tụy, tỷ lệ này tương ứng là dưới 30% và dưới 10%. Tỷ lệ tử vong cao của ung thư tuyến tụy là do không được chẩn đoán sớm và điều trị hiệu quả. Trong ung thư tuyến tụy, hầu hết các trường hợp được chẩn đoán khi bệnh đã ở giai đoạn nặng và chỉ có 20% hoặc ít hơn các bệnh nhân có khối u khu trú có khả năng chữa khỏi có thể phẫu thuật cắt bỏ. Vì vậy, việc xác định một chiến lược điều trị tiềm năng mới là cần thiết. Ngày càng có nhiều bằng chứng cho thấy mối quan hệ chặt chẽ giữa ung thư HBP và rối loạn điều hòa RON. Vì vậy, tổng quan hiện tại chủ yếu tập trung vào vai trò của RON trong cơ chế bệnh sinh của ung thư, đặc biệt là ung thư HBP. Hơn nữa, chúng tôi tóm tắt những tiến bộ mới nhất trong việc phát triển các chiến lược nhắm mục tiêu RON như một liệu pháp điều trị ung thư HBP tiềm năng.
3. Vai trò của RON và C-met trong sinh bệnh học ung thư
RON và c-MET, cả hai đều là thành viên của họ semaphorin của tyrosine kinase thụ thể xuyên màng, có chung các đặc tính cấu trúc và sinh hóa tương tự. Các protein tồn tại dưới dạng dị phân tử bao gồm các chuỗi ngoại bào và xuyên màng được liên kết với nhau bằng liên kết disulfua. Các trình tự ngoại bào RON và c-MET có các miền chức năng rất giống nhau, bao gồm SEMA, điều chỉnh quá trình phosphoryl hóa, dime hóa thụ thể và liên kết với phối tử. RON và c-MET được kích hoạt bởi các phối tử tương ứng của chúng: protein kích thích đại thực bào cho RON và protein giống yếu tố tăng trưởng tế bào gan cho c-MET. c-MET và protein giống yếu tố tăng trưởng tế bào gan được biểu hiện ở nhiều loại tế bào và mô khác nhau. Ngược lại, RON bị hạn chế chặt chẽ đối với các tế bào gốc biểu mô, trong khi tế bào gan là nguồn chính của phối tử của nó, protein kích thích đại thực bào. Sự kích hoạt độc lập hoặc phụ thuộc vào phối tử của RON và c-MET gây ra sự xâm nhập chất nền, di chuyển tế bào và tăng sinh tế bào, tất cả đều rất quan trọng đối với sự hình thành phôi, chữa lành vết thương và hình thành khối u.
Ngày càng có nhiều bằng chứng xác định vai trò của RON và c-Met trong cơ chế bệnh sinh của ung thư.
Ví dụ, c-MET và RON biểu hiện quá mức đã được quan sát thấy ở nhiều loại khối u nguyên phát và di căn, dẫn đến việc kích hoạt tín hiệu hạ lưu không bình thường, góp phần vào sự phát triển và tiến triển của ung thư. Hơn nữa, các nghiên cứu lâm sàng đã xác nhận rằng sự gia tăng biểu hiện của RON và c-MET là một yếu tố tiên lượng để dự đoán tỷ lệ sống sót và sự tiến triển của bệnh ở một số bệnh nhân ung thư. Hơn nữa, việc kích hoạt RON và c-MET thúc đẩy kiểu hình ác tính của tế bào ung thư. Biểu hiện RON và c-MET gia tăng thúc đẩy các tế bào khối u trải qua quá trình chuyển đổi từ biểu mô sang trung mô (EMT), được đặc trưng bởi sự mất đặc tính biểu mô và tăng các đặc điểm của trung mô. Sự biểu hiện c-MET và RON tăng lên cũng góp phần vào tính kháng hóa học thu được. Với vai trò nêu trên của việc gia tăng biểu hiện c-MET và RON trong sinh bệnh học ung thư, việc nhắm mục tiêu RON và c-MET thể hiện một chiến lược điều trị ung thư đầy hứa hẹn.
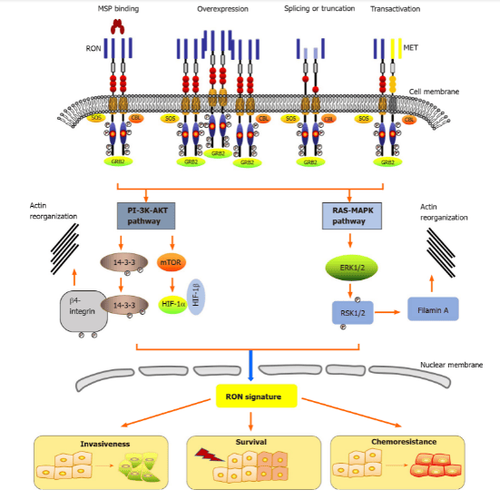
4. Các cơ chế kích hoạt và cơ chế con đường tín hiệu của ron
Tế bào biểu mô ở da, tuyến thượng thận, xương, não, thận, ruột, phổi và gan biểu hiện mức RON thấp. Hoạt động của RON đóng một vai trò quan trọng trong sự vận động của các tế bào biểu mô, tăng cường khả năng kết dính, khả năng di chuyển của tinh trùng trong mào tinh và sự phát triển của phôi thai, cũng như điều hòa các phản ứng viêm. Trong điều kiện sinh lý, nguyên nhân chính của sự hoạt hóa RON là do kích thích phối tử của nó, protein kích thích đại thực bào.
Xem thêm: Hướng dẫn chẩn đoán ung thư gan
Để đặt lịch khám tại viện, Quý khách vui lòng bấm số HOTLINE hoặc đặt lịch trực tiếp TẠI ĐÂY. Tải và đặt lịch khám tự động trên ứng dụng MyVinmec để quản lý, theo dõi lịch và đặt hẹn mọi lúc mọi nơi ngay trên ứng dụng.
Tài liệu tham khảo:
Chen SL, Wang GP, Shi DR, Yao SH, Chen KD, Yao HP. RON in hepatobiliary and pancreatic cancers: Pathogenesis and potential therapeutic targets. World J Gastroenterol 2021; 27(20): 2507-2520 [DOI: 10.3748/wjg.v27.i20.2507]