Tế bào gốc mô mỡ đã được nghiên cứu sâu rộng và cho thấy nhiều tiềm năng trong lĩnh vực y học tái tạo. Trong tương lai sẽ có nhiều nghiên cứu tiền lâm sàng và lâm sàng được tiến hành để khám phá thêm về đặc tính sinh học của loại tế bào này và mở rộng ứng dụng trong y học tái tạo. Hãy cùng tìm hiểu chi tiết về những lợi ích của tế bào gốc mô mỡ thông qua bài viết dưới đây.
Bài viết này được viết dưới sự hướng dẫn chuyên môn của các bác sĩ tại Trung tâm Công nghệ cao Vinmec thuộc Bệnh viện Đa khoa Quốc tế Vinmec.
1. Tế bào gốc mô mỡ là gì?
Tế bào gốc trung mô (MSC) là một dạng của tế bào gốc "trưởng thành". Các tế bào này có tính "đa năng", tức là có khả năng tạo ra nhiều loại tế bào chuyên biệt khác nhau trong cơ thể, dù không phải là tất cả các loại. Tế bào gốc trung mô có khả năng tạo ra các tế bào chuyên biệt tìm thấy trong mô xương, ví dụ như tế bào sụn, tế bào xương (nguyên bào xương) và tế bào mỡ. Mỗi loại tế bào chuyên biệt này sở hữu hình dạng, cấu trúc và chức năng đặc thù, mỗi tế bào sẽ thuộc về 1 mô cụ thể.
Tế bào gốc mô mỡ (ASC) được xem là tế bào gốc đa năng và đã trở thành loại tế bào phổ biến trong các ứng dụng lâm sàng gần đây. Mô mỡ (AT) mang lại lợi thế về khả năng thu hoạch, cô lập và nhân tế bào dễ dàng. Đặc biệt, mô mỡ có lượng tế bào gốc dồi dào hơn so với tủy xương.
Tế bào gốc mô mỡ có thể được thu thập từ phân đoạn mạch đệm (SVF), quá trình này diễn ra thông qua việc phân ly mô mỡ. Cả phân đoạn mạch đệm (SVF) và tế bào gốc từ mô mỡ, khi được nuôi cấy và nhân lên, đều biểu hiện các tính chất đặc trưng của tế bào gốc như khả năng biệt hóa thành nhiều loại tế bào khác nhau, khả năng tái tạo và khả năng điều hòa hệ miễn dịch.
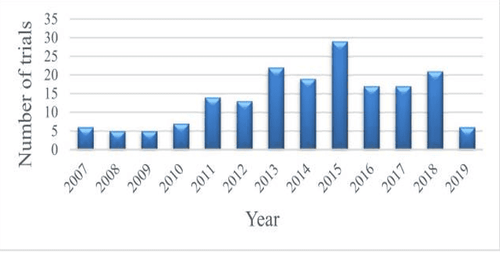
Vì thế, cả phân đoạn mạch đệm và tế bào gốc từ mô mỡ đã được nghiên cứu để đánh giá tính an toàn và hiệu quả trong ứng dụng lâm sàng cho con người. Thực tế cho thấy số lượng các thử nghiệm lâm sàng liên quan đến tế bào gốc từ mô mỡ đang tăng theo từng năm. Tuy nhiên, hầu hết các nghiên cứu này vẫn đang ở giai đoạn I và II, chúng ta vẫn còn thiếu các nghiên cứu ở giai đoạn III và IV.
2. Vai trò của tế bào gốc mô mỡ
Tế bào gốc từ mô mỡ có khả năng biệt hóa trực tiếp thành các dòng tế bào sừng, nguyên bào sợi và nội mô. Đồng thời, tế bào mô mỡ còn giải phóng các yếu tố tăng trưởng và cytokine, hỗ trợ quá trình hình thành mạch máu, phát triển, di chuyển của nguyên bào sợi, cũng như sản xuất fibronectin và collagen. Các kết quả này được xác nhận qua 14 dữ liệu từ thử nghiệm lâm sàng trên Clinicaltrial.gov. Ngoài ra, các nghiên cứu cũng chỉ ra rằng tế bào gốc mô mỡ có thể cải thiện quá trình chữa lành các vết loét mãn tính và giảm đau.
Đặc biệt, tế bào gốc từ mô mỡ còn được ứng dụng trong y học như sau:
- Tế bào gốc mô mỡ có vai trò quan trọng trong việc duy trì sự cân bằng của hệ thống miễn dịch, thông qua việc điều chỉnh tế bào T, ảnh hưởng đến hoạt động và bài tiết của IL-10. Nhờ vào khả năng này tế bào gốc từ mô mỡ được ứng dụng trong điều trị bệnh mảnh ghép chống ký chủ (GVHD).
- Tế bào gốc mô mỡ đã được chứng minh là an toàn khi áp dụng trong điều trị nhiều bệnh lý khác nhau trong suốt nhiều năm.
- Các tế bào này còn được sử dụng trong lĩnh vực y học tái tạo và điều hòa miễn dịch, nhờ vào khả năng biệt hóa thành nhiều dòng tế bào khác nhau, mang lại tiềm năng lớn cho các ứng dụng tái tạo.
- Tế bào gốc từ mô mỡ được áp dụng trong điều trị các bệnh liên quan đến tim và trong kỹ thuật mô. Liệu pháp này hỗ trợ tăng cường tái tạo mô cơ tim và cải thiện chức năng tim.
Ngoài ra, tế bào gốc từ mô mỡ còn có khả năng điều chỉnh hệ thống miễn dịch thông qua khả năng chống viêm, mang lại hiệu quả cho việc điều trị các bệnh như đa xơ cứng, xơ gan, viêm khớp dạng thấp và đái tháo đường. Tuy nhiên, một số thử nghiệm lâm sàng ngẫu nhiên có đối chứng đã cho thấy kết quả tích cực khi sử dụng tiêm tế bào gốc từ mô mỡ để điều trị thoái hóa khớp háng và khớp gối mà không gặp phải tác dụng phụ. Dưới đây là một số thử nghiệm lâm sàng nổi bật:



Một số nghiên cứu khác nổi bật liên quan tới ứng dụng liệu pháp tế bào gốc trung mô:



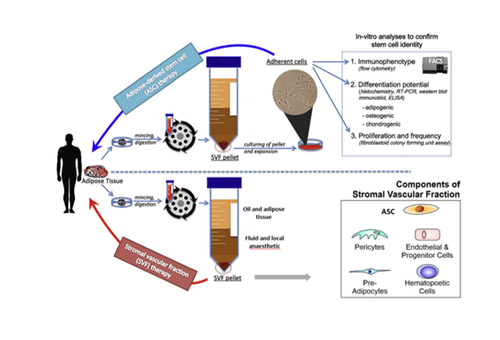
Mô mỡ có thể được thu thập 1 cách dễ dàng ở vùng bụng, sau khi trải qua quá trình phân giải bởi collagenase sẽ được chia thành 2 phần như sau:
- Tế bào mỡ.
- Phân đoạn tế bào tạo mạch nền (stromal vascular fraction - SVF).
Từ phân đoạn tế bào tạo mạch nền, các tế bào gốc mô mỡ (adipose-derived stem cells – ASC) được chọn lọc dựa trên khả năng bám dính của chúng trong môi trường nuôi cấy. Loại tế bào gốc này có khả năng biệt hóa thành các loại tế bào như mô mỡ, sụn, và xương, bên cạnh đó còn có khả năng giảm viêm nhờ vào các tác dụng paracrine.
Trong lĩnh vực ứng dụng, hiện nay cả phân đoạn tế bào tạo mạch nền và tế bào gốc từ mô mỡ đang được áp dụng trong các phòng khám và thử nghiệm lâm sàng. Phân đoạn tế bào tạo mạch nền thường được dùng cho việc tái tạo mô mềm, trong khi đó, tế bào gốc từ mô mỡ thường được nuôi cấy để tăng sinh lên từ hàng triệu đến hàng trăm triệu tế bào, phục vụ cho các ứng dụng lâm sàng cần số lượng tế bào lớn. Số lượng tế bào gốc từ mô mỡ cần thiết cho mỗi trường hợp được xác định dựa trên liều lượng sử dụng, phương thức truyền tế bào, loại bệnh được điều trị và quan trọng là kích thước của khu vực tổn thương.
Tính đến tháng 3 năm 2021, đã có 122 thử nghiệm lâm sàng sử dụng tế bào gốc mô mỡ được đăng ký trên trang “www.clinicaltrials.gov” để điều trị các bệnh liên quan đến da và mô liên kết, tim mạch, thần kinh, dinh dưỡng và chuyển hóa. Chẳng hạn, tế bào gốc mô mỡ tự thân đã được áp dụng trong điều trị tái tạo sẹo cho 8 bệnh nhân tại Khoa Bỏng và Phẫu thuật Tái tạo của Bệnh viện Đại học ở Bratislava. Sau 6 tháng điều trị, điểm trung bình trên thang điểm sẹo Vancouver (VSS) đã giảm từ 7,88 xuống còn 2,34 điểm, chứng tỏ khả năng tái tạo sẹo sau phẫu thuật của tế bào gốc từ mô mỡ.

Tế bào gốc mô mỡ tự thân cũng đã được chứng minh hiệu quả trong điều trị bệnh thoái hóa khớp. Trong một thử nghiệm lâm sàng mù đôi, phân nhóm ngẫu nhiên giai đoạn IIb, Lee và các cộng sự đã chỉ ra rằng tế bào gốc mô mỡ tự thân có thể cải thiện chức năng và giảm đau cho 12 bệnh nhân mắc viêm khớp gối mà không gây ra tác dụng phụ so với nhóm đối chứng được tiêm dung dịch muối thông thường. Đáng chú ý, tế bào gốc mô mỡ còn có khả năng tiết ra thể tiết và các túi ngoại bào (extracellular vesicles – EVs), mở ra những tiềm năng mới trong y học tái tạo và trong việc làm lành vết thương.

Các túi ngoại bào (EVs) từ tế bào gốc mô mỡ đã được chứng minh có ảnh hưởng đến quá trình hình thành mạch máu, khả năng sống và chết của tế bào, quá trình viêm nhiễm và tái tạo mô, cũng như giảm các tình trạng bệnh lý. Kwon và các cộng sự đã áp dụng thể tiết từ tế bào gốc mô mỡ hỗ trợ điều trị sẹo mụn bằng laser CO2 phân đoạn cho 25 bệnh nhân trong 12 tuần. Kết quả cho thấy, việc kết hợp thể tiết từ mô mỡ với phương pháp laser CO2 phân đoạn tăng hiệu quả điều trị, (giảm số điểm đánh giá sẹo mụn ECCA - échelle d’évaluation clinique des cicatrices d’acné scores - là 32.5% so với 19,9%; cũng như giảm tỉ lệ ban đỏ và thời gian điều trị)
Trong hơn 20 năm qua, mô mỡ và tế bào gốc từ mô mỡ đã được nghiên cứu rộng rãi và được coi là nguồn tế bào đầy tiềm năng trong kỹ thuật mô và y học tái tạo. Trong tương lai, dự kiến sẽ có thêm nhiều nghiên cứu tiền lâm sàng và lâm sàng được tiến hành nhằm khám phá thêm về đặc tính sinh học và mở rộng các ứng dụng của tế bào mô mỡ trong lĩnh vực y học tái tạo.
3. Vinmec nghiên cứu và ứng dụng liệu pháp tế bào gốc mô mỡ trong điều trị bệnh mãn tính
Theo kịp xu hướng hiện đại, Vinmec là một trong những đơn vị tiên phong tại Việt Nam trong việc nghiên cứu và ứng dụng liệu pháp tế bào gốc để điều trị các bệnh lý mãn tính chưa có phương pháp điều trị hiệu quả. Một trong những loại tế bào gốc được nghiên cứu và ứng dụng tại Vinmec là tế bào gốc trung mô từ mô mỡ tự thân.
Vào năm 2014, Vinmec đã tiến hành nghiên cứu về việc sử dụng tế bào gốc từ mô mỡ để điều trị các bệnh thoái hóa khớp và chấn thương cột sống. Đến năm 2017, Vinmec đã tiến hành một thử nghiệm lâm sàng nhãn mở, đơn nhóm để đánh giá an toàn và hiệu quả của việc sử dụng tế bào gốc trung mô từ mô mỡ trong điều trị suy giảm nội tiết tố sinh dục sớm ở người trung niên.
Nghiên cứu đã hoàn thành việc thu thập và tổng kết số liệu, cho thấy những kết quả ban đầu về hiệu quả và an toàn của liệu pháp điều trị. Các ưu điểm và công nghệ nổi bật của Vinmec bao gồm:
Vinmec đã hoàn toàn làm chủ công nghệ phân lập và nuôi cấy tế bào gốc mô mỡ. Quá trình nuôi cấy tế bào gốc diễn ra trong hệ thống phòng sạch đạt tiêu chuẩn ISO 14644-1 (Class 6, Class 7 và Class 8), đảm bảo môi trường vô trùng tối ưu cho việc phân lập, xử lý và nuôi cấy tế bào. Chất lượng của tế bào gốc được kiểm chuẩn bằng hệ thống xét nghiệm nghiêm ngặt theo các tiêu chuẩn quốc tế.
Vinmec cũng sở hữu một Ngân hàng sinh học hiện đại đạt tiêu chuẩn quốc tế, cho phép lưu trữ tế bào gốc trung mô từ mô mỡ. Điều này cho phép tái sử dụng tế bào gốc cho các lần điều trị tiếp theo mà không cần thực hiện lại thủ thuật thu thập mô mỡ, từ đó giảm chi phí và rủi ro cho bệnh nhân.
Tóm lại, tế bào gốc mô mỡ vẫn đang được tiếp tục nghiên cứu trong các dự án tiền lâm sàng và lâm sàng để khám phá đặc tính sinh học và mở rộng ứng dụng của chúng trong lĩnh vực y học tái tạo.
Để đặt lịch khám tại viện, Quý khách vui lòng bấm số HOTLINE hoặc đặt lịch trực tiếp TẠI ĐÂY. Tải và đặt lịch khám tự động trên ứng dụng MyVinmec để quản lý, theo dõi lịch và đặt hẹn mọi lúc mọi nơi ngay trên ứng dụng.
Tài liệu tham khảo:
Patricia A. Zuk MZ, Hiroshi Mizuno, Jerry Huang, J. William Futrell, Adam J. Katz, Prosper Benhaim, H. Peter Lorenz, Marc H. Hedrick. Multilineage Cells from Human Adipose Tissue: Implications for Cell-Based Therapies. Tissue Engineering. 2001;7(2):211-28.
Zuk PA, Zhu M, Ashjian P, Ugarte DAD, Huang JI, Mizuno H, et al. Human Adipose Tissue Is a Source of Multipotent Stem Cells. Molecular biology of the cell. 2002;13(12):4279-95.
Patrikoski M, Mannerstrom B, Miettinen S. Perspectives for Clinical Translation of Adipose Stromal/Stem Cells. 2019;2019:5858247.
Laloze J, Varin A, Bertheuil N, Grolleau JL, Vaysse C, Chaput B. Cell-assisted lipotransfer: Current concepts. Annales de Chirurgie Plastique Esthétique. 2017;62(6):609-16.
Garcia-Olmo D, Herreros D, Pascual I, Pascual JA, Del-Valle E, Zorrilla J, et al. Expanded adipose-derived stem cells for the treatment of complex perianal fistula: a phase II clinical trial. Diseases of the colon and rectum. 2009;52(1):79-86.
Zahorec P, Sarkozyova N, Ferancikova N, Bukovcan P, Danisovic L, Bohac M, et al. Autologous mesenchymal stem cells application in post-burn scars treatment: a preliminary study. Cell and tissue banking. 2021;22(1):39-46.
Lee WS, Kim HJ, Kim KI. Intra-Articular Injection of Autologous Adipose Tissue-Derived Mesenchymal Stem Cells for the Treatment of Knee Osteoarthritis: A Phase IIb, Randomized, Placebo-Controlled Clinical Trial. 2019;8(6):504-11.
Wong DE, Banyard DA, Santos PJF, Sayadi LR, Evans GRD, Widgerow AD. Adipose-derived stem cell extracellular vesicles: A systematic review(✰). Journal of plastic, reconstructive & aesthetic surgery : JPRAS. 2019;72(7):1207-18.
Kwon HH, Yang SH, Lee J, Park BC, Park KY, Jung JY, et al. Combination Treatment with Human Adipose Tissue Stem Cell-derived Exosomes and Fractional CO2 Laser for Acne Scars: A 12-week Prospective, Double-blind, Randomized, Split-face Study. Acta dermato-venereologica. 2020;100(18):adv00310.
Gimble JM, Guilak F. Adipose-derived adult stem cells: isolation, characterization, and differentiation potential. Cytotherapy. 2003;5(5):362-9.
Lindroos B, Suuronen R, Miettinen S. The Potential of Adipose Stem Cells in Regenerative Medicine. Stem Cell Reviews and Reports. 2011;7(2):269-91.
Oedayrajsingh-Varma MJ, van Ham SM, Knippenberg M, Helder MN, Klein-Nulend J, Schouten TE, et al. Adipose tissue-derived mesenchymal stem cell yield and growth characteristics are affected by the tissue-harvesting procedure. Cytotherapy. 2006;8(2):166-77.
Mesenchymal stem cells: the "other" bone marrow stem cells; https://www.eurostemcell.org/mesenchymal-stem-cells-other-bone-marrow-stem-cells.
Lalu M.M., McIntyre L., Pugliese C., Fergusson D., Winston B.W., Marshall J.C., Granton J., Stewart D.J. Safety of cell therapy with mesenchymal stromal cells (SafeCell): a systematic review and meta-analysis of clinical trials. PLoS ONE. 2012;7:e47559. doi: 10.1371/journal.pone.0047559. [PMC free article] [PubMed] [CrossRef] [Google Scholar].
Joo H.J., Kim J.-H., Hong S.J. Adipose Tissue-Derived Stem Cells for Myocardial Regeneration. Korean Circ. J. 2017;47:151–159. doi: 10.4070/kcj.2016.0207. [PMC free article] [PubMed] [CrossRef] [Google Scholar].
Bai X., Yan Y., Song Y.-H., Seidensticker M., Rabinovich B., Metzele R., Bankson J.A., Vykoukal D., Alt E. Both cultured and freshly isolated adipose tissue-derived stem cells enhance cardiac function after acute myocardial infarction. Eur. Heart J. 2009;31:489–501. doi: 10.1093/eurheartj/ehp568. [PubMed] [CrossRef] [Google Scholar].
Haenel A., Ghosn M., Karimi T., Vykoukal J., Kettlun C., Shah D., Dave A., Valderrabano M., Schulz D., Azares A. Unmodified, autologous adipose-derived regenerative cells improve cardiac function, structure and revascularization in a porcine model of chronic myocardial infarction. bioRxiv. 2018 doi: 10.1101/286468. [CrossRef] [Google Scholar].
Park M.-J., Kwok S.-K., Lee S.-H., Kim E.-K., Park S.-H., Cho M.-L. Adipose tissue-derived mesenchymal stem cells induce expansion of interleukin-10-producing regulatory B cells and ameliorate autoimmunity in a murine model of systemic lupus erythematosus. Cell Transplant. 2015;24:2367–2377. doi: 10.3727/096368914X685645. [PubMed] [CrossRef] [Google Scholar].
Dall’Oca C., Breda S., Elena N., Valentini R., Samaila E.M., Magnan B. Mesenchymal Stem Cells injection in hip osteoarthritis: Preliminary results. Acta Bio-Med. Atenei Parm. 2019;90:75–80. [PMC free article] [PubMed] [Google Scholar].
Jones I.A., Wilson M., Togashi R., Han B., Mircheff A.K., Vangsness C.T., Jr. A randomized, controlled study to evaluate the efficacy of intra-articular, autologous adipose tissue injections for the treatment of mild-to-moderate knee osteoarthritis compared to hyaluronic acid: A study protocol. BMC Musculoskelet. Disord. 2018;19:383. doi: 10.1186/s12891-018-2300-7. [PMC free article] [PubMed] [CrossRef] [Google Scholar].
Lee W.-S., Kim H.J., Kim K.-I., Kim G.B., Jin W. Intra-Articular Injection of Autologous Adipose Tissue-Derived Mesenchymal Stem Cells for the Treatment of Knee Osteoarthritis: A Phase IIb, Randomized, Placebo-Controlled Clinical Trial. Stem Cells Transl. Med. 2019 doi: 10.1002/sctm.18-0122. [PMC free article] [PubMed] [CrossRef] [Google Scholar].
Roato I., Belisario D.C., Compagno M., Lena A., Bistolfi A., Maccari L., Mussano F., Genova T., Godio L., Perale G. Concentrated adipose tissue infusion for the treatment of knee osteoarthritis: Clinical and histological observations. Int. Orthop. 2019;43:15–23. doi: 10.1007/s00264-018-4192-4. [PubMed] [CrossRef] [Google Scholar].
Adipose Tissue Stem Cells for Therapy: An Update on the Progress of Isolation, Culture, Storage, and Clinical Application. J Clin Med. 2019 Jul; 8(7): 917. Published online 2019 Jun 26. doi: 10.3390/jcm8070917.