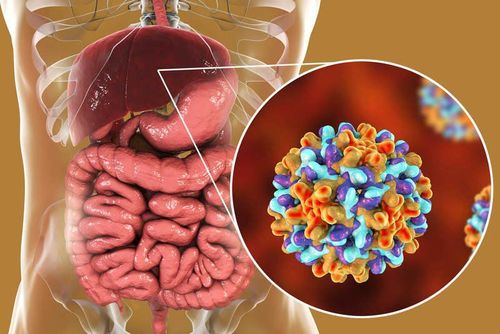
Nhiễm viêm gan C (HCV) là thành viên duy nhất của chi Hepacivirus trong họ Flaviviridae, mã hóa bộ gen RNA mạch đơn dương được dịch thành một chuỗi polypeptide lớn duy nhất, sau đó được xử lý bằng phương pháp thủy phân protein để tạo ra các protein vi-rút riêng lẻ, tất cả đều rất quan trọng đối với quá trình lây nhiễm tối ưu của vi-rút.
Bài viết được viết bởi ThS.BS Mai Viễn Phương - Bác sĩ nội soi tiêu hóa, Khoa Khám bệnh & Nội khoa - Bệnh viện Đa khoa Quốc tế Vinmec Central Park.
Mối nguy hại khi nhiễm viêm gan siêu vi C (HVC)
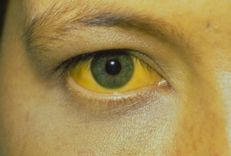
Nhiễm viêm gan C (HCV) là một vấn đề sức khỏe toàn cầu có thể dẫn đến xơ gan, HCC hoặc thậm chí tử vong. Nhiễm viêm gan C lây truyền qua đường máu. Bệnh thường được phát hiện dưới dạng nhiễm trùng mãn tính ở cả nhóm phụ nữ mang thai và không mang thai. Phụ nữ mang thai có thể truyền HCV cho trẻ sơ sinh trong tử cung hoặc trong thời kỳ quanh sinh; nhiễm trùng trong thời kỳ mang thai có liên quan đến việc tăng nguy cơ cho thai nhi, bao gồm hạn chế sự phát triển của thai nhi và cân nặng khi sinh thấp. Ở những vùng lưu hành, tình trạng đồng nhiễm HCV/HBV rất phổ biến và những bệnh nhân đồng nhiễm có nguy cơ mắc HCC, xơ gan, xơ gan và các bệnh gan khác cao hơn.
Vào đầu năm 2020, ước tính số ca nhiễm viêm gan siêu vi C HCV trên toàn thế giới là 56,8 triệu: Giảm so với năm 2015. Dữ liệu dịch tễ học từ Hoa Kỳ cho thấy tỷ lệ mắc viêm gan C ngày càng tăng ở phụ nữ trong độ tuổi sinh đẻ; ước tính có 1%-4% phụ nữ mang thai bị nhiễm HCV, từ đó gây ra nguy cơ lây truyền từ mẹ sang con khoảng 5%. Ngoài ra, viêm gan C mãn tính (CHC) được cho là ảnh hưởng đến khoảng 2,4 triệu người. Tuy nhiên, nhiễm HCV phổ biến hơn từ 3 đến 20 lần ở những bệnh nhân mắc các bệnh tâm thần nghiêm trọng, chẳng hạn như rối loạn trầm cảm nặng, rối loạn nhân cách, rối loạn lưỡng cực hoặc tâm thần phân liệt, so với những nhóm dân số không mắc các bệnh này. Người ta cũng đã xác định rõ ràng rằng nhiễm HCV phổ biến hơn nhiều ở tù nhân so với dân số nói chung
HCV vẫn phổ biến ở những người sử dụng thuốc tiêm tĩnh mạch và việc lây truyền thường liên quan đến hành vi tiêm chích có nguy cơ. Do đó, nó có vẻ phổ biến ở một số nhóm người hiến máu, với tỷ lệ đồng nhiễm HCV cao. Nó có tỷ lệ lây truyền từ mẹ sang con cao, nhưng vì nó gây ra rất ít hoặc thậm chí không gây bệnh ở trẻ sơ sinh bị nhiễm bệnh nên không cần sàng lọc trước sinh
IFN loại I và các dạng miễn dịch bẩm sinh tế bào khác sẽ ngăn chặn sự sao chép của vi-rút và các tác nhân gây bệnh khác, tạo thành cơ sở cho việc sử dụng IFNα liên hợp trong việc quản lý CHC. HCV ức chế dạng miễn dịch này như một biện pháp đối phó, thông qua việc sử dụng nhiều sản phẩm gen khác nhau như protease HCV, vai trò chính của nó là xử lý polyprotein vi-rút lớn thành các protein riêng lẻ có chức năng cụ thể
Trong tình trạng đồng nhiễm HCV/HBV, HCV chiếm ưu thế và ức chế sự nhân lên của HBV. Các protein lõi HCV và IFN được HCV kích hoạt có tác dụng ức chế HBV.Tình trạng ức chế miễn dịch cũng đã được quan sát thấy ở những bệnh nhân đồng nhiễm HCV và HBV. Giảm phản ứng kháng thể trung hòa HCV và lưu thông tế bào hỗ trợ nang T giống Th1 được thấy ở những bệnh nhân đồng nhiễm HCV và HBV
Xét nghiệm huyết thanh có thể hỗ trợ chẩn đoán, sử dụng xét nghiệm phân tử khi cần thiết để hướng dẫn quản lý viêm gan C. Tuy nhiên, do tiến triển âm thầm và không có bất kỳ triệu chứng lâm sàng giai đoạn đầu đáng kể nào, CHC thường chỉ được chẩn đoán sau khi xơ gan và HCC phát triển.
Điều trị viêm gan siêu vi C (HCV)
Tiến trình chữa khỏi viêm gan C (HCV) diễn ra chậm chạp kể từ khi phát hiện ra bệnh vào năm 1989, và các lựa chọn điều trị trước đây dựa trên peg-IFNα, có liên quan đến các tác dụng phụ về mặt thần kinh; do đó, điều này khiến những bệnh nhân mắc bệnh tâm thần nặng bị loại khỏi chương trình điều trị HCV, các chương trình loại trừ và các thử nghiệm lâm sàng. Tuy nhiên, đã có những tiến bộ đáng kể trong điều trị HCV, bao gồm sự ra đời của các liệu pháp chữa khỏi. Kể từ năm 2014, việc chấp thuận các tác nhân kháng vi-rút tác dụng trực tiếp (DAA) đường uống an toàn, được dung nạp tốt đã dẫn đến sự thay đổi mô hình trong điều trị nhiễm HCV và các DAA này thậm chí có thể loại trừ nhiễm HCV.
Đối với liệu pháp HCV lựa chọn đầu tiên, các hướng dẫn gần đây khuyến nghị các loại thuốc có tác dụng trên toàn bộ kiểu gen ( tức là các loại thuốc có hiệu quả trên tất cả các kiểu gen HCV). Các phác đồ DAA hứa hẹn chữa khỏi HCV với 8-12 tuần điều trị một lần mỗi ngày được dung nạp tốt[ 88 ]. Hiệu quả cao và khả năng kháng thuốc thấp của DAA đã giúp chữa khỏi CHC, khiến WHO đề xuất một chương trình loại trừ viêm gan siêu vi trên toàn cầu. Nhiều quốc gia đã áp dụng các sáng kiến để loại trừ HCV, đến mức việc loại trừ HCV hiện là vấn đề cung cấp dịch vụ chăm sóc sức khỏe. Liệu pháp DAA cho các bệnh nhiễm trùng viêm gan C tái phát sau LT có liên quan đến đáp ứng vi-rút kéo dài (SVR) gần 100%, bất kể kiểu gen. Ngoài ra, liệu pháp này khả thi đối với những bệnh nhân mắc CKD hoặc bệnh thận giai đoạn cuối cần chạy thận nhân tạo và có tỷ lệ chữa khỏi cao mà không cần điều chỉnh liều. Liệu pháp DAA đơn độc có thể điều trị viêm cầu thận cryoglobulinemia liên quan đến HCV, trong khi liệu pháp kháng vi-rút và ức chế miễn dịch đồng thời là cần thiết trong các trường hợp liên quan đến các biểu hiện nghiêm trọng, đe dọa cơ quan của cryoglobulinemia.
Mặt khác, mặc dù tỷ lệ diệt trừ HCV thành công cao, nguy cơ các biến cố liên quan đến gan vẫn còn ngay cả sau khi chữa khỏi HCV, chẳng hạn như HCC, đây là biến chứng chính của nhiễm HCV; những bệnh nhân có nguy cơ mắc HCC nên được theo dõi HCC liên tục. Các tác nhân DAA đã được sử dụng an toàn trong các điều kiện huyết học. Chúng nên được xem xét để sử dụng như một phương pháp điều trị đơn lẻ đầu tay trong các bệnh u lympho indolent, kết hợp với hóa trị liệu trong các trường hợp hung hãn. Việc điều trị nhiễm HCV ở trẻ em đang hoạt động (HCV-RNA dương tính) hiện nay rất đơn giản và dễ dàng vì nhiều phác đồ DAA đã được chấp thuận cho trẻ em trên ba tuổi. Việc sàng lọc viêm gan C trong thời kỳ mang thai và việc quản lý sau đó vẫn là vấn đề chưa được giải quyết, nhưng việc đưa thuốc DAA vào sử dụng có thể mang tính cách mạng nếu có thể xác định được tính an toàn của chúng trong thời kỳ mang thai. Việc cho con bú cũng được coi là an toàn đối với phụ nữ bị viêm gan C
Về phác đồ DAA, các nghiên cứu thực tế cho thấy SVR của sofosbuvir (SOF)/daclatasvir (DCV) là chấp nhận được và có thể sử dụng để điều trị HCV thành công. Tuy nhiên, việc sử dụng SOF/DCV bị hạn chế do thời gian điều trị dài hơn ở bệnh nhân kiểu gen-3, cũng như nhu cầu sử dụng ribavirin (RBV) ở những bệnh nhân đã từng điều trị, dẫn đến nguy cơ gặp tác dụng phụ cao hơn. DCV có khả năng vẫn được sử dụng để điều trị như một lựa chọn cho việc điều trị bệnh nhân kiểu gen-1, kiểu gen-2 và kiểu gen-4 trong điều kiện nguồn lực hạn chế, trong khi bệnh nhân kiểu gen-3 có nhiều khả năng được hưởng lợi từ các phối hợp DAA không có RBV như phác đồ velpatasvir (VEL)/SOF trong 12 tuần hoặc phác đồ glecaprevir/pibrentasvir (GLE/PIB) trong 8 tuần.
Ở 98% bệnh nhân, liệu pháp kết hợp GLE/PIB, VEL/SOF và các liệu pháp DAA khác đã được chứng minh là thành công trong việc tiêu diệt vi-rút, ngay cả trong những trường hợp mà các phương pháp điều trị trước đó đã thất bại hoặc có sự thay thế liên quan đến kháng thuốc. Hiện đang có cuộc tranh luận tập trung vào viêm gan C và kỳ vọng về việc sử dụng DAA uống một lần mỗi ngày toàn bộ kiểu gen HCV mới được chấp thuận, GLE/PIB và SOF/VEL/voxilaprevir. Mặt khác, việc quản lý những bệnh nhân HCV khó chữa bao gồm những cá nhân đã thất bại với các DAA trước đó, người dùng ma túy tiêm tĩnh mạch và những bệnh nhân bị xơ gan mất bù hoặc suy thận
Các tác dụng phụ trong quá trình điều trị DAA rất hiếm hoặc nhẹ, và những bệnh nhân có bệnh đi kèm như xơ gan còn bù thường đủ điều kiện để điều trị. Tuy nhiên, ngay cả sau khi điều trị lại, một tỷ lệ nhỏ bệnh nhân vẫn không loại bỏ được vi-rút. Thất bại này thường chủ yếu là do đột biến xóa NS5A P32 xuất hiện sau liệu pháp DAA ban đầu ở những bệnh nhân kiểu gen-1b, mặc dù lý do thất bại vẫn chưa được biết ở một số bệnh nhân. Ở những bệnh nhân này, có thể thử các liệu pháp thay thế như SOF cộng với RBV, không dựa vào chất ức chế NS5A. Các nỗ lực điều trị mở rộng quy mô đặt ra một thách thức và một phần của vấn đề là nhiều người mang vi-rút đơn giản là không biết rằng họ đã bị nhiễm.
Điều này có thể dẫn đến tổn thương gan không thể phục hồi trong thời gian dài và nếu bệnh nhân không được chẩn đoán kịp thời, họ có thể tiếp tục phát triển HCC hoặc suy gan ngay cả sau khi vi-rút đã được loại bỏ. Liệu pháp DAA bị bù đắp một phần bởi tình trạng lạm dụng thuốc tiêm tĩnh mạch ngày càng tăng. Mặt khác, liệu pháp DAA phải được cá nhân hóa cho những bệnh nhân mất bù, cân nhắc đến các hướng dẫn hiện hành và đề xuất của các hiệp hội như Hiệp hội Nghiên cứu Gan Châu Âu hoặc Hiệp hội Nghiên cứu Bệnh gan Hoa Kỳ
Trong nhiễm trùng đồng thời HCV/HBV, cả hai loại vi-rút đều tương tác trong gan; việc điều trị các nhiễm trùng đồng thời này dựa trên kiểu gen và phức tạp, do sự tương tác giữa các loại vi-rút. Điều trị các trường hợp HCV chiếm ưu thế sử dụng thuốc DAA và peg-IFN cộng với RBV, theo dõi liên tục aspartate aminotransferase (AST) và alanine aminotransferase (ALT). Điều trị các trường hợp HBV chiếm ưu thế ít gặp hơn sử dụng peg-IFN và NUC, theo dõi AST và ALT.
Tỷ lệ SVR ở nhiễm trùng đồng thời HCV/HBV cao hơn so với nhiễm trùng đơn khi được điều trị bằng thuốc DAA, nhưng có nguy cơ HBV có thể tái hoạt động trong hoặc sau khi điều trị. Tái hoạt động ít phổ biến hơn ở những bệnh nhân được điều trị bằng thuốc DAA so với những bệnh nhân được điều trị bằng peg-IFN cộng với RBV. HBcrAg, HBV DNA, RNA tiền gen của HBV và các dấu ấn sinh học HBV khác không hiệu quả trong việc dự đoán sự tái hoạt động của HBV; chỉ có nồng độ HBsAg đóng vai trò là dấu ấn sinh học hiệu quả cho sự tái hoạt của HBV. HCV cũng có thể phản ứng, nhưng chỉ được thấy trong những trường hợp rất hiếm khi HBV hiện diện và được điều trị trước. Ngoài ra, giống như HBV, bệnh nhân ung thư bị nhiễm HCV có nguy cơ tái hoạt vi-rút cao sau khi điều trị ung thư. Tuy nhiên, vẫn còn rất ít dữ liệu về sự tái hoạt của HCV ở những bệnh nhân ung thư đã được điều trị bằng thuốc ức chế điểm kiểm soát miễn dịch và các loại thuốc chống ung thư mới hơn khác
Tính đến thời điểm viết bài này, vắc-xin CHC vẫn đang được nghiên cứu. Do đó, việc giảm thiểu các nguồn lây nhiễm là một bước quan trọng hướng tới việc loại bỏ CHC ngoài việc cắt đứt các con đường lây truyền, điều này đòi hỏi phải sàng lọc, chẩn đoán và điều trị cho càng nhiều dân số càng tốt. Các chiến lược sàng lọc tại bệnh viện đã được chứng minh là hiệu quả về mặt chi phí trong việc quản lý sàng lọc CHC, như đã báo cáo cả trong nước và quốc tế. Ngoài ra, LT là giải pháp cuối cùng duy nhất được bảo hành cho bệnh xơ gan mất bù do HCV. Mặt khác, đối với bệnh nhân CKD, nhiễm viêm gan siêu vi C (HCV) có hậu quả bất lợi về gan, thận và tim mạch, bao gồm cả bệnh nhân đang điều trị chạy thận nhân tạo hoặc đã ghép thận
Tài liệu tham khảo
1. Cooke GS, . Accelerating the elimination of viral hepatitis: a Lancet Gastroenterology & Hepatology Commission. Lancet Gastroenterol Hepatol. 2019;4:135-184
2. Sinn DH, Cho EJ, Kim JH, Kim DY, Kim YJ, Choi MS. Current status and strategies for viral hepatitis control in Korea. Clin Mol Hepatol. 2017;23:189-195
3. Usuda D, et allCurrent perspectives of viral hepatitis. World J Gastroenterol 2024; 30(18): 2402