Bài được viết bởi Thạc sĩ, Bác sĩ Bùi Thị Hồng Khang - Bác sĩ Giải phẫu bệnh - Khoa Xét nghiệm - Bệnh viện Đa khoa Quốc tế Vinmec Central Park.
Các tác nhân sinh ung được xếp vào 3 nhóm chính: Các hoá chất, bức xạ và virus. Chúng có thể tác động riêng rẽ hoặc hiệp đồng với nhau. Trong bài viết này, chúng ta sẽ đề cập đến các virus sinh u.
1. Virus ARN sinh u
Tất cả các virus ARN sinh u đều thuộc về họ Retrovirus, nghĩa là chúng có chứa enzyme sao chép ngược (reverse transcriptase), cho phép sao chép ARN của virus thành ADN. Cấu tạo di truyền của Retrovirus là một mạch đơn ARN, có chứa các gen pol mã hóa cho enzyme sao chép ngược, gen gag mã hóa cho protein capsid và gen env mã hóa cho protein vỏ bao. Ngoài ra, ở về phía hai đầu 3’và 5’còn có 2 đoạn LTR (long terminal repeats) dài khoảng 250 - 1200 nucleotide, chứa các yếu tố điều hòa cần thiết cho hoạt động của retrovirus như tổ hợp gen vào bộ gen tế bào chủ, tổng hợp protein.
Tùy theo khả năng gây chuyển dạng các tế bào động vật nuôi cấy nhanh hay chậm (sau vài tuần hoặc vài tháng), virus ARN sinh u được phân thành 2 loại như sau.
1.1. Virus ARN sinh u gây chuyển dạng nhanh (acute transforming oncogenic RNA virus)
Khả năng gây chuyển dạng nhanh của các virus này là do bộ gen của chúng có chứa các gen gây chuyển dạng, gọi là gen virus sinh u, hoặc oncogene-virus (viral oncogene), viết tắt là v-onc. Thí dụ: v-sis là oncogene của retrovirus gây sarcôm ở khỉ (simian sarcoma virus), v-fes là oncogene của retrovirus gây sarcôm ở loài mèo (feline sarcoma virus). Cấu tạo của bộ gen các retrovirus này đều gồm có các gen env, v-onc, gag và 2 đoạn LTR ở 2 đầu. Những loại retrovirus không gây chuyển dạng thì không chứa các oncogen trong bộ gen của chúng.
Các phân tử protein mã hóa bởi oncogene được tổng hợp, gọi là oncoprotein, có khả năng chuyển dạng tế bào nuôi cấy thành tế bào ung thư; vì vậy, còn được gọi là yếu tố chuyển dạng (transforming factor).
Bằng kỹ thuật lai ghép phân tử (molecular hybridization), người ta rất ngạc nhiên khi phát hiện trong ADN của tế bào người bình thường cũng có chứa các gen tương tự với oncogene virus; các gen này được gọi là tiền-oncogene (proto-oncogene); thí dụ: Tiền-oncogene tương tự v-sis được gọi là sis, được tìm thấy trên nhiễm sắc thể 22, tiền-oncogene tương tự v-fes là fes nằm trên nhiễm sắc thể 15.
Các tiền-oncogene cũng được tìm thấy ở hầu hết các loài sinh vật, từ sinh vật cấp thấp cho đến loài người. Sự bảo tồn các gen này trong suốt quá trình tiến hoá chứng tỏ các tiền-oncogene rất cần thiết cho sự tăng trưởng và biệt hoá của tế bào bình thường. Khi cấu trúc tiền-oncogene bị thay đổi hoặc khi sự biểu hiện của nó lệch lạc, tiền-oncogene được hoạt hoá thành oncogene-tế bào, viết tắt là c-onc (cellular oncogene), có thể gây rối loạn tăng sinh tế bào, dẫn đến sự hình thành u.
Dựa vào phát hiện trên, người ta cho rằng các retrovirus sinh u gây chuyển dạng nhanh khởi đầu có cấu tạo bộ gen giống các retrovirus không gây chuyển dạng khác, nghĩa là không có chứa các v-onc. Các v-onc này là kết quả của sự tái tổ hợp ngẫu nhiên giữa bộ gen của virus và ADN của tế bào chủ bình thường, nhờ đó, các tiền-oncogene trong bộ gen của tế bào chủ được chuyển sang bộ gen của virus và biến thành các v-onc.
1.2. Virus ARN sinh u gây chuyển dạng chậm (slow transforming oncogenic RNA virus)
Loại virus này không chứa các v-onc; sau khi xâm nhập vào tế bào nuôi cấy, toàn bộ bộ gen của virus được sao chép ngược thành ADN, gọi là tiền virus (provirus) và được tổ hợp ngẫu nhiên vào bộ gen của tế bào chủ. Nếu tiền virus ngẫu nhiên được gắn kết gần với một tiền-oncogene thì dưới tác dụng của yếu tố điều hòa nằm trong chuỗi LTR của tiền virus, tiền-oncogene của tế bào chủ có thể bị hoạt hóa thành oncogene-tế bào, đưa đến sự chuyển dạng tế bào. Do tính chất ngẫu nhiên này mà phải mất vài tháng mới có tác động gây chuyển dạng.
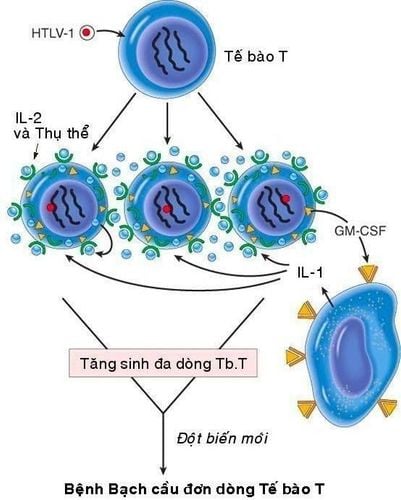
Mặc dù trên động vật thực nghiệm đã phát hiện được nhiều loại retrovirus có khả năng sinh u nhưng đối với người thì chỉ mới xác định được 1 loại retrovirus có khả năng gây ung thư là virus HTLV-1 (human T-cell leukemia virus type 1), gây ra bệnh bạch cầu tế bào T tuýp 1. Đây là bệnh thường gặp ở một số vùng của Nhật Bản và vịnh Caribe. Virus HTLV-1 sau khi xâm nhập vào người sẽ tấn công và gây chuyển dạng các lympho bào T CD4+; 1% số người nhiễm virus sẽ phát bệnh bạch cầu đơn dòng tế bào T sau thời gian tiềm ẩn từ 20 - 30 năm.
Cấu trúc bộ gen của HTLV-1 cũng có chứa các gen gag, pol, env và LTR như các retrovirus khác. Ngoài ra, còn có thêm 1 gen tax ở đầu 3’. Cơ chế gây ung thư của HTLV-1 không giống với 2 loại virus ARN sinh u đã nói trên; bởi vì nó không chứa các v-onc và cũng không được tổ hợp ngẫu nhiên vào cạnh một tiền-oncogene nào của tế bào chủ.
Khả năng gây ung thư của HTLV-1 là do hoạt động của gen tax: Protein tax có khả năng hoạt hoá một số gen của tế bào chủ, thí dụ như gen mã hoá cho IL-2 và thụ thể tương ứng, gen mã hoá cho GM-CSF. Khi vào được cơ thể, virus HTLV-1 xâm nhập và kích thích sự tăng sinh nhiều dòng tế bào T theo kiểu tự tiết (qua sự sản xuất IL-2 và thụ thể tương ứng) hoặc cận tiết (qua sự sản xuất GM-CSF kích thích đại thực bào sản xuất IL-1). Sự tăng sinh đa dòng tế bào T tạo thuận lợi cho việc xảy ra các đột biến mới, làm xuất hiện 1 dòng tế bào T tăng sinh trội hơn, dẫn đến ung thư.
Ung thư là nguyên nhân gây tử vong hàng thứ 2 trên thế giới. Thử sức cùng bài trắc nghiệm sau đây sẽ giúp bạn có thêm kiến thức về yếu tố nguy cơ cũng như cách phòng ngừa bệnh ung thư.
Bài dịch từ: webmd.com
2. Virus ADN sinh u
Đến nay, chỉ có 3 loại virus ADN được xác định là có khả năng gây ung thư ở người. Khi xâm nhập vào tế bào, ADN của virus thường được tổ hợp bền vững với ADN của tế bào chủ. Nhờ đó, ta có thể phát hiện ra sự hiện diện của chúng bằng kỹ thuật lai ghép phân tử.
2.1. Các papillomavirus ở người (HPV)
Papillomavirus là loại virus ADN có ái tính với tế bào biểu mô, có thể gây ra u nhú ở da và niêm mạc. Papillomavirus có hình cầu đường kính 55nm, cấu tạo gồm 1 vỏ bao protein 20 mặt (capsid), bên trong chứa 1 phân tử ADN xoắn kép vòng dài khoảng 8000 cặp baz, gồm có 2 vùng: Vùng mang gen gồm 6 gen biểu hiện sớm là E1, E2, E4, E5, E6, E7 và 2 gen biểu hiện muộn, L1, L2; vùng còn lại không mang gen nhưng chứa các yếu tố điều hoà cần thiết cho hoạt động của HPV trong tế bào chủ.

Khi biểu mô lát tầng bị nhiễm HPV (thí dụ ở cổ tử cung), virus chỉ gắn kết được với màng tế bào của lớp đáy để xâm nhập vào bên trong. Vì vậy, phải có một vết rách trong biểu mô để virus có thể tiếp cận. Khi đã vào trong nhân của tế bào đáy, 2 tình huống có thể xảy ra:
- Nhiễm khuẩn tiềm ẩn: HPV tồn tại “yên lặng” dưới dạng ADN vòng nằm ngoài nhiễm sắc thể của tế bào chủ, với số lượng 50 - 100 bản. ADN vòng của virus chỉ được tái bản một lần cho mỗi chu kỳ tế bào đáy. Ở biểu mô bị nhiễm khuẩn tiềm ẩn, không có bất kỳ biến đổi hình thái tế bào nào cho biết đang bị nhiễm HPV.
- Nhiễm khuẩn hoạt động: Gen E6 và E7 của virus được biểu hiện khiến tế bào đáy sau khi đã biệt hoá về hình thái và di chuyển lên lớp cận đáy thì vẫn giữ được khả năng tái bản ADN, đồng thời, cho phép ADN của virus tái bản. Trong các tế bào của lớp trung gian, các gen E1, E2, E4 và E5 sẽ thúc đẩy ADN của virus tái bản mạnh mẽ. Gen L1 và L2 được biểu hiện muộn hơn, tạo ra protein capsid để tổ hợp với ADN virus thành các HPV mới. Gen E4 phá huỷ các siêu sợi cytokeratin trong bào tương, giúp phóng thích HPV ra khỏi lớp tế bào bề mặt. Hình ảnh tế bào rỗng ở lớp trung gian là kết quả của sự phá huỷ bộ xương tế bào, tạo ra 1 khoảng sáng trong bào tương quanh nhân.
Hiện nay, đã phân lập hơn 100 tuýp HPV khác nhau:
- HPV tuýp 1, 2, 4, 7, gây u nhú da lành tính.
- HPV có ái tính vùng sinh dục - hậu môn, gồm khoảng 40 tuýp khác nhau; có thể gây ra tổn thương trong biểu mô với nguy cơ chuyển thành ung thư. HPV lây lan chủ yếu qua đường tình dục. Tình trạng nhiễm HPV rất phổ biến, 80% phụ nữ ở độ tuổi 20 bị nhiễm HPV, có thể nhiều tuýp khác nhau cùng lúc nhưng đến 50 tuổi thì tỉ lệ này chỉ còn 5%. May mắn là đa số các trường hợp nhiễm HPV chỉ có tính tạm thời, sẽ biến mất sau 1 - 2 năm do tác động của hệ miễn dịch; chỉ những trường hợp nhiễm HPV tồn tại kéo dài mới làm tăng nguy cơ ung thư. Tuỳ theo nguy cơ này ít hay nhiều, ta có thể phân biệt 2 nhóm: Nhóm nguy cơ thấp như HPV tuýp 6, 11, 42, 44, 53, 54, 62, 66, gây ra condylom sùi hoặc tổn thương trong biểu mô gai grade thấp (LSIL); nhóm nguy cơ cao gồm HPV tuýp 16, 18, 31, 33, 35, 39, 45, 51, 52, 56, 58, 59, 68, gây ra các tổn thương trong biểu mô gai grade cao (HSIL) có khả năng tiến triển thành ung thư xâm nhập.
Cơ chế gây ung thư của HPV là do bộ gen của virus đã được tổ hợp ngẫu nhiên vào ADN của tế bào chủ, gây rối loạn hoạt động của các gen tại đó; trong khi ở các tổn thương tiền ung, bộ gen của virus vẫn nằm riêng biệt bên ngoài. Hoạt động của gen E6 sẽ bất hoạt các protein p53 và protein bax, đồng thời tái hoạt hóa enzyme telomerase, tế bào chủ dù có mang đột biến gen chẳng những không tự huỷ mà lại còn được bất tử hoá. Gen E7 ức chế protein Rb, giải phóng các yếu tố điều hoà sao chép, thúc đẩy tế bào chủ tăng sinh. Kết quả, tế bào chủ bị chuyển dạng thành tế bào có khả năng tăng sinh tự động, phá vỡ màng đáy và xâm nhập vào mô xung quanh. Tuy nhiên, sự nhiễm HPV đơn thuần có lẽ chưa đủ để gây ra ung thư mà còn cần thêm một số đột biến gen khác (chẳng hạn như đột biến tiền-oncogene ras), nay đã dễ xảy ra hơn do bộ gen tế bào chủ không còn ổn định như lúc chưa bị nhiễm virus.

2.2. Virus Epstein-Barr (Epstein-Barr virus - EBV)
Là virus thuộc họ Herpes, được xem là nguyên nhân gây ra 2 loại ung thư là lymphoma Burkitt và carcinôm không biệt hoá của vòm hầu.
Lymphoma Burkitt hay gặp ở một số vùng của Châu Phi, người ta đã tìm thấy ADN của EBV trong tế bào ung thư của tất cả các bệnh nhân này. EBV có ái tính mạnh với các limpho bào B, sau khi xâm nhập sẽ kích thích lympho bào B tăng sinh. Trong cơ thể bình thường, sự tăng sinh limphô bào B được kiểm soát nhưng ở những bệnh nhân bị suy giảm miễn dịch (do mắc bệnh sốt rét hoặc nhiễm trùng), cơ chế kiểm soát không còn hiệu quả; các lympho bào B tiếp tục tăng sinh, tạo thuận lợi cho sự xảy ra các đột biến mới, làm xuất hiện một dòng lympho bào B tăng sinh trội hơn, dẫn đến lymphoma Burkitt.
Carcinôm không biệt hoá của vòm hầu là ung thư thường gặp ở vùng Đông Nam Á và Trung Quốc. Người ta đã tìm thấy ADN của EBV trong tế bào ung thư của tất cả các bệnh nhân mắc loại ung thư này. Tương tự như trong lymphoma Burkitt, EBV có thể đã tương tác với một số yếu tố khác để gây ra carcinôm không biệt hoá của vòm hầu.
2.3. Virus viêm gan B (HBV)
Các nghiên cứu dịch tễ học cho thấy có mối liên hệ chặt chẽ giữa tình trạng nhiễm HBV mạn tính với ung thư gan. Cơ chế gây ung thư của HBV vẫn chưa được biết rõ mặc dù có sự tổ hợp giữa ADN của virus và ADN tế bào chủ. Cơ chế sinh u của HBV có lẽ thông qua khả năng gây tổn thương làm chết tế bào gan khiến các tế bào gan còn lại phải tăng sinh liên tục, tạo thuận lợi cho sự xuất hiện các đột biến mới dẫn đến ung thư.
Ngoài các virus trên, gần đây đã xác định được vai trò của vi khuẩn Helicobacter pylori (Hp) trong 2 loại ung thư dạ dày là carcinôm tuyến và lymphoma tế bào B. Cơ chế gây ung thư của Hp có lẽ thông qua khả năng gây viêm dạ dày mãn tính; dẫn đến chuyển sản ruột, nghịch sản và cuối cùng là carcinôm tuyến. Sự tăng sinh đa dòng tế bào lympho B trong viêm dạ dày mãn tính tạo thuận lợi cho việc xảy ra các đột biến mới, làm xuất hiện một dòng tế bào B tăng sinh trội hơn, dẫn đến lymphoma dạ dày.
Tóm lại, nghiên cứu về các virus sinh u đã giúp chúng ta phát hiện ra sự tồn tại của các tiền-oncogene ở người mà đến nay đã biết hơn 100 loại khác nhau. Mặc dù đa số các loại ung thư ở người không phải do virus trực tiếp gây ra nhưng chính sự hoạt hoá các tiền-oncogene cùng với sự bất hoạt nhiều loại gen khác nữa đã gây ra chuyển dạng tế bào soma, dẫn đến sự hình thành các khối u.
Hãy theo dõi trang web: Vinmec.com thường xuyên để cập nhật nhiều thông tin hữu ích khác.
Để đặt lịch khám tại viện, Quý khách vui lòng bấm số HOTLINE hoặc đặt lịch trực tiếp TẠI ĐÂY. Tải và đặt lịch khám tự động trên ứng dụng MyVinmec để quản lý, theo dõi lịch và đặt hẹn mọi lúc mọi nơi ngay trên ứng dụng.