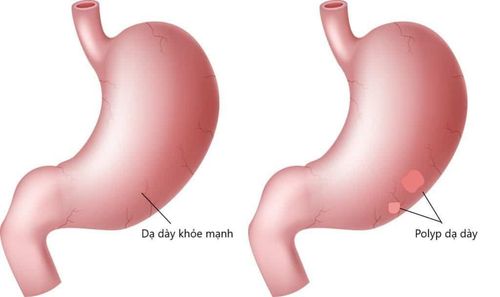
Polyp dạ dày (GP) là các tổn thương trong lòng dạ dày xuất hiện phía trên bề mặt niêm mạc. Định nghĩa đơn giản này bao gồm nhiều loại tổn thương với nhiều loại mô học và tiềm năng tân sinh khác nhau.
Việc phát hiện GP đang ngày càng trở nên phổ biến trong thực hành lâm sàng, với tỷ lệ mắc bệnh hiện tại ước tính là 6% trong các thủ thuật nội soi đường tiêu hóa trên. Polyp dạ dày nguy cơ ác tính thấp bao gồmcác polyp có nguy cơ ác tính thấp như polyp tăng sản, u tuyến, khối u thần kinh nội tiết loại 1 và 2 và HaP.
Polyp dạ dày tăng sản
Polyp tăng sản dạ dày (GHP) là polyp biểu mô phổ biến được tìm thấy trong dạ dày, với tỷ lệ mắc bệnh dao động từ 15% ở những khu vực ít nhiễm H. pylori đến 75% ở những quần thể nhiễm H. pylori lan rộng. GHP là phản ứng với các kích thích viêm mãn tính, chủ yếu do nhiễm H. pylori , cũng như viêm teo dạ dày mãn tính, thiếu máu ác tính, lỗ thông dạ dày và các vị trí loét và xói mòn
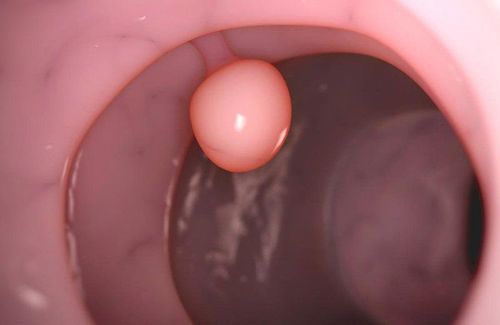
Polyp tăng sản dạ dày không biểu hiện khuynh hướng ở nam hay nữ; tuy nhiên, chúng thường ảnh hưởng đến những cá nhân ở giai đoạn giữa đến cuối cuộc đời. Trên nội soi thực quản dạ dày, polyp tăng sản dạ dày có thể xuất hiện ở nhiều dạng khác nhau, từ bề mặt trơn láng đến phân thùy, và có thể không cuống hoặc có cuống, với kích thước thường nhỏ hơn 2 cm, mặc dù kích thước lớn hơn lên tới 12 cm đã được báo cáo. Chúng thường có bề mặt màu đỏ và thường bị xói mòn, đặc biệt là khi chúng phát triển về kích thước (Hình 1 ).
Các đặc điểm hình thái của GHP có thể khiến việc phân biệt chúng với tăng sản nang dạng polyp hoặc polyp tuyến dạ dày trở nên khó khăn, nhấn mạnh sự cần thiết của việc lấy mẫu sinh thiết. Hang vị là vị trí bị ảnh hưởng phổ biến nhất ở dạ dày (60%), mặc dù Polyp tăng sản dạ dày có thể xuất hiện ở bất kỳ vùng nào của dạ dày, bao gồm cả tâm vị. Chúng có thể xuất hiện dưới dạng các khối u đơn độc hoặc phổ biến hơn là các khối u nhiều.
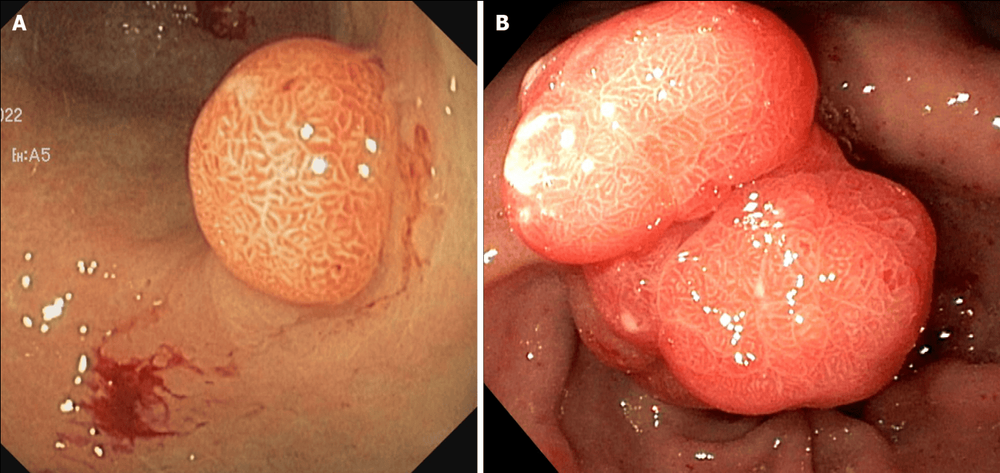
Polyp tăng sản dạ dày thường không có triệu chứng và được phát hiện tình cờ trên nội soi thực quản dạ dày. Tuy nhiên, chúng có thể gây chảy máu khi bị xói mòn hoặc tắc nghẽn đường ra dạ dày từng đợt khi có cuống và sa từ hang vị vào bóng vị. Về mặt vi thể, Polyp tăng sản dạ dày được đặc trưng bởi các tuyến nang hình nang dài, giãn nở, phân nhánh, méo mó với tế bào chất nhầy và mô đệm bị viêm
Polyp tăng sản dạ dày từ lâu đã được coi là khối u lành tính, tuy nhiên, sự phát triển của chúng trong bối cảnh viêm mãn tính có thể làm tăng nguy cơ chuyển dạng tân sinh, theo trình tự u tuyến-ung thư biểu mô.
Khi kiểm tra mô học, 15% GHP biểu hiện loạn sản ruột, trong khi gần 5% biểu hiện dấu hiệu loạn sản và ung thư hiện diện ở dưới 1% . Đáng chú ý, Polyp tăng sản dạ dày lớn hơn 1 cm, biểu hiện hình thái có cuống, xuất hiện ở những cá nhân đã cắt dạ dày hoặc cùng tồn tại với các tổn thương tân sinh khác, tất cả đều là những yếu tố khiến Polyp tăng sản dạ dày dễ chuyển dạng tân sinh.
U tuyến dạ dày
U tuyến dạ dày (GA) chiếm 6% đến 10% tổng số GP ở các nước phương Tây, với tỷ lệ cao hơn ở các nước như Nhật Bản và Trung Quốc. Viêm teo dạ dày và loạn sản ruột thường là nguyên nhân gây ra các polyp này, mặc dù chúng cũng có thể xảy ra ở những bệnh nhân không mắc các tình trạng viêm dạ dày.
Không có mối liên hệ nào được xác nhận với nhiễm trùng H. pylori và không có bằng chứng nào cho thấy điều trị bằng PPI làm tăng nguy cơ phát triển GA.
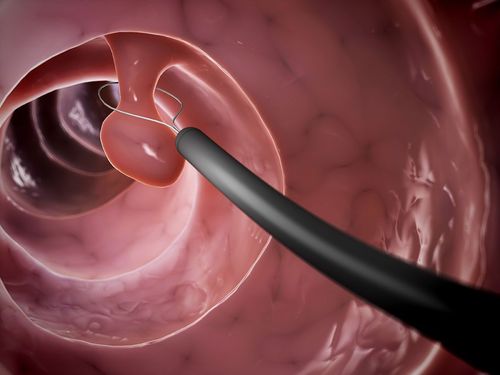
Trên nội soi thực quản dạ dày, chúng thường là các tổn thương đơn lẻ có thể phẳng, không cuống hoặc có hình dạng cuống, với kích thước dao động từ vài milimét đến cm (Hình 2 ).
Không giống như u tuyến đại tràng, kiểu hố của u tuyến dạ dày được quan sát thấy qua nội soi sắc ký và độ phóng đại không tương quan với bệnh lý mô học của tổn thương. Về mặt vi thể, có bốn loại U tuyến dạ dày: Loại ruột, loại foveolar, loại tuyến môn vị và loại tuyến oxyntic
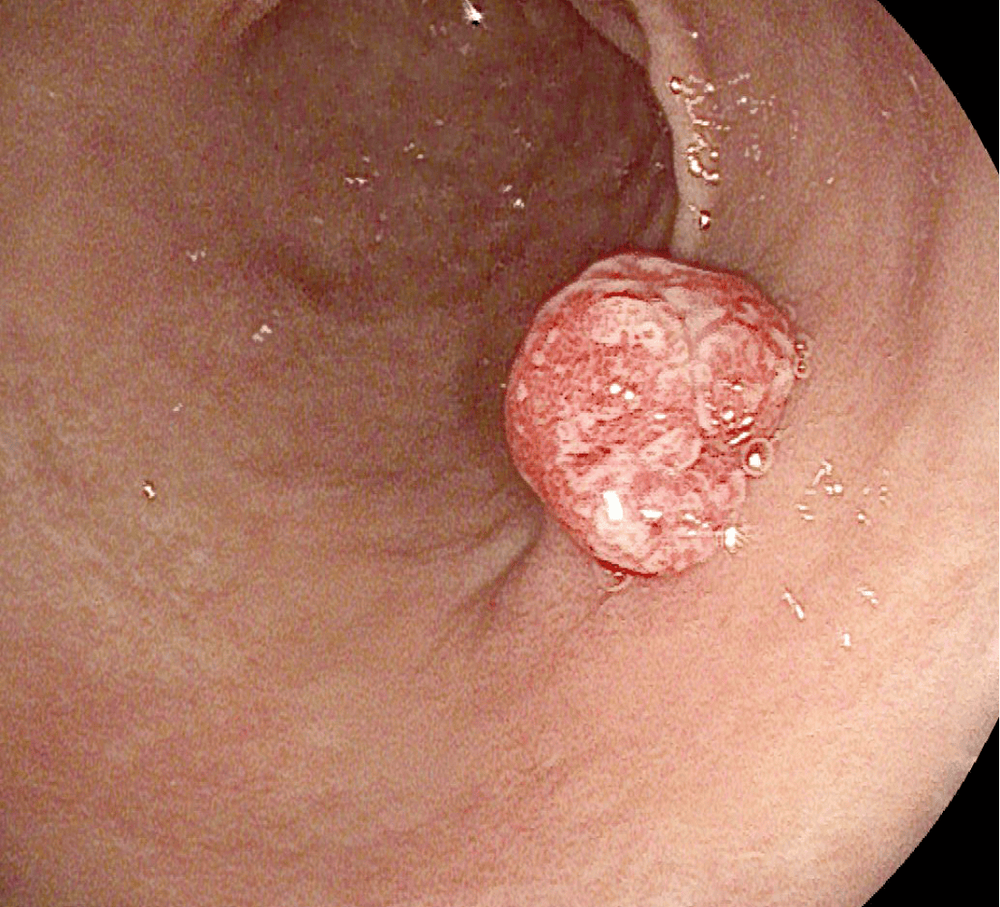
Khối u thần kinh nội tiết dạ dày
U thần kinh nội tiết dạ dày (G-NET) bao gồm các khối u thần kinh nội tiết biệt hóa tốt được tìm thấy trong dạ dày. Cùng với một tỷ lệ nhỏ các ung thư biểu mô thần kinh nội tiết biệt hóa kém, chúng tạo nên các khối u thần kinh nội tiết dạ dày (G-NEN).
Tổ chức Y tế Thế giới chia G-NET thành ba cấp độ mô học (G1, G2, G3) tùy thuộc vào tỷ lệ nguyên phân và chỉ số ki-67. Ngoài ra, G-NET biệt hóa tốt được phân thành ba loại lâm sàng (loại 1, loại 2 và loại 3) theo nguyên nhân, hành vi và tiên lượng.
Để đánh giá G-NET, điều cần thiết là phải sinh thiết polyp, hang vị và thân/đáy dạ dày, vì điều này có thể cung cấp thông tin về nguyên nhân và tiên lượng của khối u. Sinh thiết polyp đánh giá cấp độ của khối u, trong khi cần nhớ rằng NET thường nằm sâu trong niêm mạc.
Khối u thần kinh nội tiết loại 1
G-NET loại 1 phát triển khi có tăng sản tế bào ECL do nồng độ gastrin tăng cao trong viêm teo dạ dày tự miễn. Những khối u này chiếm tới 80% tất cả các G-NEN. Trong quá trình OGD, G-NET loại 1 biểu hiện dưới dạng các polyp nhỏ, đỏ và nhiều, chủ yếu nằm ở đáy và thân dạ dày (Hình 3 ).
Niêm mạc xung quanh, cần lấy mẫu, biểu hiện teo tế bào niêm mạc, tăng sản tế bào thần kinh nội tiết và suy giảm tế bào thành. Lấy mẫu dịch dạ dày để đo pondus hydrogenii (pH) cho thấy mức pH cao.
Xét nghiệm máu cho thấy mức gastrin huyết thanh tăng, thiếu vitamin B12 có hoặc không có thiếu máu hồng cầu to và 80% dương tính với kháng thể kháng tế bào thành. Nồng độ Chromogranin A (CgA) tăng cao nhưng không hữu ích như một dấu hiệu khối u.
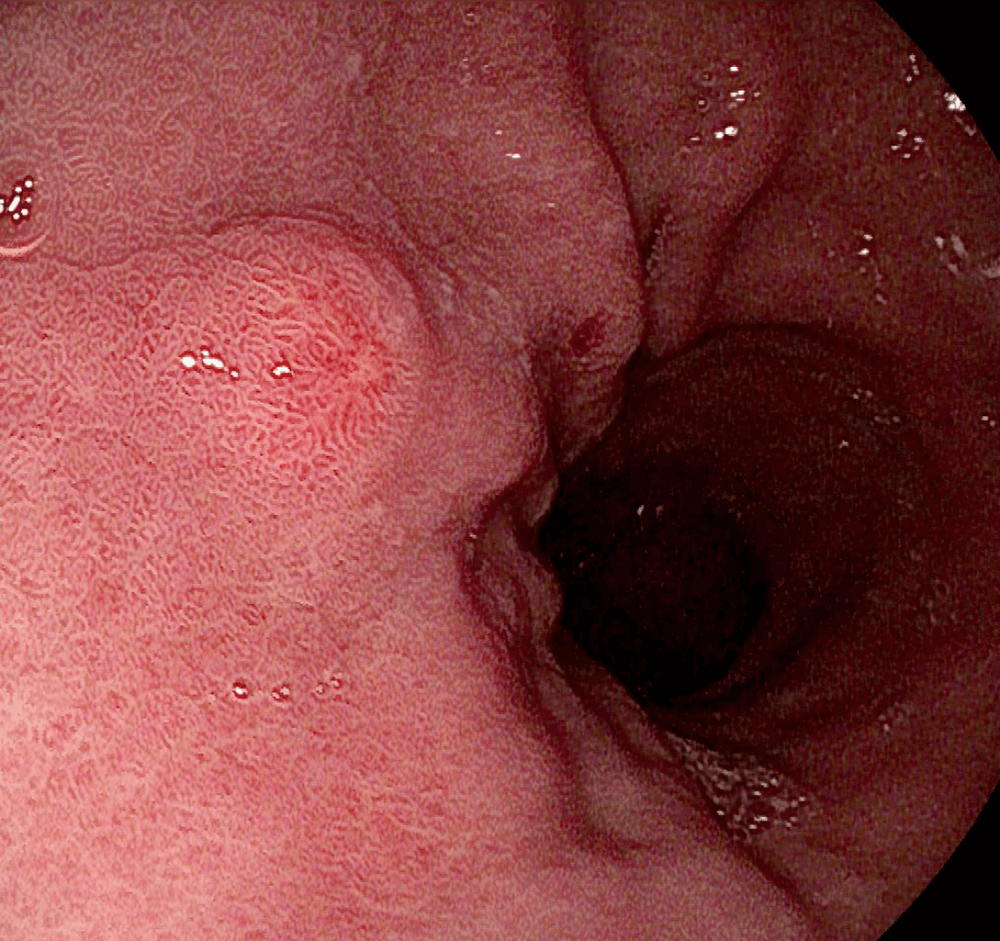
Trong trường hợp G-NET loại 1, tiên lượng thường là tích cực, với nguy cơ di căn dưới 1% ở các khối u nhỏ hơn 10 mm. Phẫu thuật cắt bỏ được khuyến nghị đối với các tổn thương có kích thước từ 10 mm trở lên. Đối với G-NET loại 1 nhỏ hơn 10 mm, khuyến cáo nên theo dõi nội soi thường xuyên sau mỗi 6 tháng và sau đó là 12 tháng một lần. Không cần sinh thiết lại nếu các đặc điểm của polyp vẫn không thay đổi.
Siêu âm qua nôi soi (EUS) được khuyến cáo cho các khối u > 1 cm và những khối u có độ G2 bất kể kích thước tổn thương, để xác định độ sâu của xâm lấn và sự liên quan của hạch bạch huyết. Chụp cắt lớp cắt ngang với chụp cộng hưởng từ (MRI) và chụp cắt lớp vi tính ngực bụng có cản quang (CT), và chụp chức năng với chụp cắt lớp phát xạ positron thụ thể somatostatin (PET)/CT (68Ga-SSA-PET-CT), chỉ được yêu cầu trong các trường hợp di căn hoặc các đặc điểm nguy cơ cao (G2 trên sinh thiết, mạch máu hoặc xâm lấn bạch huyết, nghi ngờ T2 trên EUS) hoặc biên độ R1 sau khi cắt bỏ nội soi
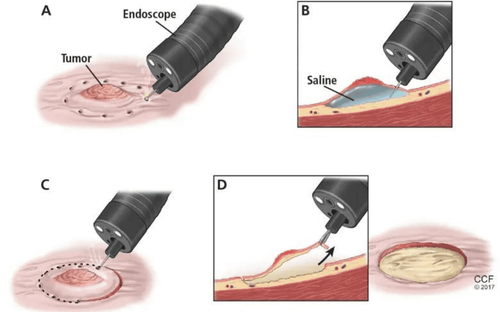
Đối với G-NET loại 1, phương pháp điều trị được lựa chọn là cắt bỏ nội soi bao gồm cắt bỏ niêm mạc nội soi (EMR), bóc tách dưới niêm mạc nội soi (ESD) và cắt bỏ toàn bộ độ dày (FTR). Mặc dù ESD và FTR dẫn đến tỷ lệ cắt bỏ R0 cao hơn, nhưng lựa chọn kỹ thuật không được chuẩn hóa và phụ thuộc vào vị trí, đặc điểm của tổn thương và chuyên môn tại địa phương. Theo các tuyên bố hướng dẫn được công bố gần đây của Hiệp hội U thần kinh nội tiết Châu Âu, trong các trường hợp cắt bỏ R1, nên áp dụng phương pháp tiếp cận tăng dần (EMR > ESD > FTR > phẫu thuật). Sau khi cắt bỏ R0 G-NET loại 1, nên lên lịch theo dõi bằng nội soi thực quản dạ dày sau 1 năm.
Mặc dù hiếm gặp, khối u có kích thước > 20 mm hoặc nghi ngờ xâm lấn cơ, nên phẫu thuật lấy mẫu hạch bạch huyết. Các chất tương tự somatostatin có thể được sử dụng liên tục ở những bệnh nhân mắc bệnh di căn hoặc ở những bệnh nhân không đủ điều kiện để cắt bỏ bằng phẫu thuật.
U thần kinh nội tiết loại 2
G-NET loại 2 tạo nên một phân nhóm nhỏ hơn, ít phổ biến hơn của G-NET (khoảng 5%). Tương tự như G-NET loại 1, sản xuất quá mức gastrin dẫn đến phì đại và tăng sản của các tế bào ECL. Tuy nhiên, trong trường hợp của G-NET loại 2, gastrin được tiết ra bởi u gastrin liên quan đến hội chứng Zollinger-Ellison, thường xảy ra ở những bệnh nhân mắc hội chứng tân sinh nội tiết đa dạng loại 1 (MEN-1).
Trên nội soi dạ dày trên, G-NET loại 2 xuất hiện dưới dạng các polyp nhỏ, nhiều và màu vàng, chủ yếu nằm ở thân dạ dày và đáy dạ dày, thường được bao quanh bởi loét dạ dày tá tràng. Về mặt mô học, niêm mạc xung quanh bình thường, phì đại hoặc viêm nhẹ nhưng không teo. Hơn nữa, đo độ pH của dịch dạ dày cho thấy độ pH thấp do tăng axit clohydric. Bệnh nhân có thể bị tiêu chảy, phân mỡ, đau bụng và xuất hiện chảy máu do loét dạ dày tá tràng. Khi nghi ngờ G-NET loại 2, cần xét nghiệm máu với nồng độ parathormone, canxi, gastrin và insulin để loại trừ khả năng mắc MEN.
So với G-NET loại 1, G-NET loại 2 có xu hướng ảnh hưởng đến những bệnh nhân trẻ tuổi hơn và có nguy cơ di căn hạch bạch huyết cao hơn (khoảng 30%), mặc dù tiên lượng chung là thuận lợi. Phương pháp điều trị tối ưu cho G-NET loại 2 vẫn chưa được thiết lập chắc chắn và phụ thuộc vào việc quản lý hội chứng MEN-1.
Đối với G-NET lớn hơn 10 mm, nên cân nhắc cắt bỏ sau khi đánh giá EUS trước đó, trong khi các tổn thương nhỏ hơn 10 mm có thể được theo dõi thông qua giám sát nội soi thực quản dạ dày. Các lựa chọn điều trị bao gồm cắt bỏ nội soi hoặc phẫu thuật bao gồm cắt dạ dày một phần hoặc toàn bộ.
HaPs (Polyp Hamartomatous)
Polyp Hamartomatous (HaP) dạ dày là một loại polyp dạ dày hiếm gặp, chiếm khoảng 1% trong số tất cả các polyp dạ dày. Polyp Hamartomatous thường liên quan đến các hội chứng như hội chứng Peutz-Jeghers (PJS), hội chứng polyp vị thành niên (JPS), đồng đẳng phosphatase và tensin và hội chứng hamartoma. JPS là hội chứng polyp đường tiêu hóa di truyền phổ biến nhất, với tỷ lệ mắc bệnh là 1/100000-160000. Đây là một rối loạn trội trên nhiễm sắc thể thường do đột biến ở gen SMAD4 , BMPRA1 hoặc ENG.
Trên nội soi thực quản dạ dày, Polyp Hamartomatous chủ yếu xuất hiện dưới dạng polyp dạ dày cố định, đơn độc hoặc nhiều polyp, về mặt hình thái giống với polyp tăng sản. Đôi khi thấy một khối phình dưới niêm mạc được bao phủ bởi niêm mạc dạ dày bình thường với một chỗ lõm màu đỏ hoặc không đều ở phía trên. Về mặt mô học, chúng là kết quả của sự phát triển không theo trật tự của các mô bản địa tại vị trí đó, bắt nguồn từ bất kỳ lớp phôi nào trong 3 lớp và được hình thành từ các tuyến oxyntic giãn nở dạng nang và các tuyến oxyntic biến dạng không đều.
Polyp Hamartomatous rải rác còn được gọi là HaP đảo ngược dạ dày (GIHP). Đây là những tổn thương dưới niêm mạc đặc trưng bởi sự phát triển đảo ngược của các tuyến dạ dày trên mô học.
Tài liệu tham khảo
1. Park DY, Lauwers GY. Gastric polyps: classification and management. Arch Pathol Lab Med. 2008;132:633-640.
2. Carmack SW, Genta RM, Schuler CM, Saboorian MH. The current spectrum of gastric polyps: a 1-year national study of over 120,000 patients. Am J Gastroenterol. 2009;104:1524-1532
3. Costa D, Ramai D, Tringali A. Novel classification of gastric polyps: The good, the bad and the ugly. World J Gastroenterol 2024; 30(31): 3640-3653