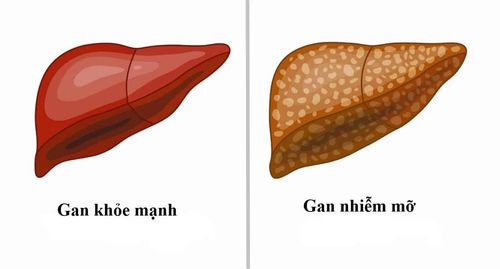
Bệnh gan nhiễm mỡ không do rượu (NAFLD) được mô tả là loại bệnh gan mãn tính phổ biến nhất trên toàn thế giới. bệnh gan nhiễm mỡ không do rượu được coi là nguyên nhân ngày càng tăng của các rối loạn gan giai đoạn cuối trên toàn thế giới và nổi lên như một bệnh lý học của ung thư biểu mô tế bào gan (HCC) ngay cả khi xơ gan tiềm ẩn không có.
Bài viết được viết bởi ThS. BS Mai Viễn Phương - Trưởng đơn nguyên Nội soi tiêu hóa - Khoa Khám bệnh & Nội khoa - Bệnh viện Đa khoa Quốc tế Vinmec Central Park.
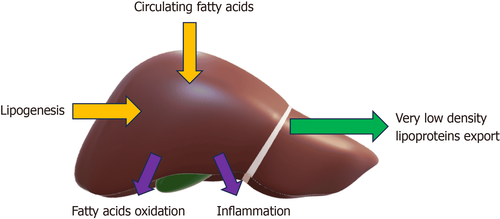
Trên thực tế, sự tích tụ quá mức lipid trong tế bào gan (dưới dạng triglyceride, hàm lượng chất béo > 5% trong gan; được gọi là mỡtosis) của những người uống rượu ở mức độ nguy cơ thấp là đặc điểm chính của bệnh nhân bệnh gan nhiễm mỡ không do rượu. Pyroptosis, ferroptosis và necroptosis là các phân nhóm chính của các trường hợp chết tế bào không do apoptosis (RCD), mỗi loại đều biểu hiện các đặc điểm riêng.
Tổng quan về pyroptosis
Zychlinsky và cộng sự ban đầu đã báo cáo về pyroptosis vào những năm 1990 và mô tả một dạng chết tế bào ly giải ở các đại thực bào bị nhiễm Shigella flexneri . Tuy nhiên, thuật ngữ 'pyroptosis' xuất hiện vào năm 2001 khi các nhà khoa học tiết lộ rằng cái chết của các đại thực bào do Salmonella gây ra phụ thuộc vào caspase (CASP)-1. Sau đó, số lượng CASP liên quan đến pyroptosis đối lập với CASP liên quan đến apoptosis đã tăng lên đáng kể và bao gồm CASP-1, CASP-11 và các CASP-4 và CASP-5 tương ứng ở người. Đáng ngạc nhiên là tác nhân gây apoptosis nổi tiếng CASP-3 được coi là CASP pyroptosis trong các điều kiện cụ thể. Về cơ bản, loại Chết tế bào theo chương trình này xảy ra sau khi các tác nhân gây bệnh nội bào gây nhiễm trùng dẫn đến hình thành các lỗ màng tế bào phụ thuộc vào hoạt động của CASP, sưng tấy, vỡ tế bào và giải phóng các interleukin gây viêm như interleukin (IL)-1β và IL-18.
Gasdermin D tạo lỗ (GSDMD) được mô tả vào năm 2015 đóng vai trò là tác nhân gây ra pyroptosis. Mảnh GSDMDNT đầu N 31-KDa được tạo ra khi GSDMD bị cắt bởi tác động của CASP-1 và CASP-11. GSDMDNT thể hiện hoạt động tạo lỗ nội tại. Hơn nữa, quá trình cắt GSDMD tạo ra mảnh GSDMDCT đầu C 22-kDa. Mảnh này gắn vào GSDMDNT để ức chế protein. Việc điều hòa tăng GSDMDNT một mình được theo sau bởi sự cảm ứng của pyroptosis, tuy nhiên, GSDMDCT ngăn chặn pyroptosis do GSDMDNT gây ra. Điều quan trọng là, có tài liệu chứng minh rằng GSDMD thuộc về một họ protein lớn hơn bao gồm GSDMA đến GSDME (còn được gọi là DFNA5) và DFNB59. Các cuộc điều tra gần đây cho thấy GSDME hoạt động như một kẻ hành quyết pyroptosis khác, có khả năng chuyển đổi apoptosis do CASP-3 trung gian thành pyroptosis. Phần lớn GSDM có liên quan đến tỷ lệ mắc và phát triển của nhiều loại bệnh, tuy nhiên, cơ chế kích hoạt phân tử và chức năng chính xác vẫn chủ yếu chưa được biết đến.

Hai con đường truyền tín hiệu bao gồm tín hiệu chuẩn và không chuẩn kích hoạt pyroptosis
Hai tín hiệu này khác nhau ở ứng dụng của phức hợp đa protein trong tế bào chất được gọi là inflammasome. Inflammasome kích hoạt con đường chuẩn của pyroptosis. Về mặt này, inflammasome có thể nhận ra các tín hiệu nguy hiểm nội sinh và ngoại sinh khác nhau như các mẫu phân tử liên quan đến mầm bệnh (PAMP) và DAMP. Inflammasome chuẩn bao gồm một protein cảm biến thuộc miền liên kết nucleotide (NBD), protein giống như speck liên quan đến apoptosis chứa CARD (ASC), thụ thể giống AIM2 hoặc họ NLR (chứa lặp lại giàu leucine) hoặc pyrin và pro-CASP-1 là một zymogen không hoạt động. Khi inflammasome chính thống được hình thành, sự hoạt hóa của CASP-1 dẫn đến sự phân cắt pro-IL-1β và pro-IL-18 thành các dạng hoạt động của chúng. Tiếp theo, hai IL này được giải phóng ra ngoài tế bào sau tác động của GSDMDNT gây ra sự hình thành bào tử trong màng tế bào. Trong khi đó, con đường không chính thống phụ thuộc vào CASP-11 mà không có sự mồi inflammasome sẽ phân cắt GSDMD. Trong loại pyroptosis này, GSDMDNT truyền tín hiệu trở lại inflammasome NLRP3 chính thống dẫn đến sự hoạt hóa của con đường phụ thuộc CASP-1.
Pyroptosis có thể góp phần vào sự tiến triển của bệnh gan nhiễm mỡ không do rượu và chuyển sang NASH
Nhiều yếu tố như độc tính mỡ, rối loạn chức năng ty thể, căng thẳng lưới nội chất, con đường chết tế bào gan và phản ứng miễn dịch bẩm sinh có thể khởi phát các quá trình viêm mãn tính ở gan, có thể cung cấp nhiên liệu cho quá trình chuyển đổi từ NAFL sang NASH. Sự thâm nhiễm của đại thực bào và hoạt hóa các tế bào Kupffer tại chỗ được coi là đặc điểm chính của bệnh sinh học. Yếu tố hoại tử khối u (TNF)-α được giải phóng bởi các tế bào Kupffer nuôi dưỡng một vòng luẩn quẩn của các phản ứng viêm và khởi phát xơ hóa sau khi kích hoạt apoptosis. Tuy nhiên, gần đây đã xuất hiện rằng các CASP gây viêm như CASP-4/5 ở người, CASP-1 và CASP-11 ở chuột đóng vai trò quan trọng như các chất trung gian gây viêm. Do đó, người ta cho rằng pyroptosis có liên quan rất lớn đến sự phát triển của NAFLvà tiến triển thành NASH.
Có tài liệu chứng minh rằng sự hoạt hóa của inflammasome bởi các yếu tố điển hình như axit uric, DAMP và axit béo, làm tăng biểu hiện của các thành phần NLRP3, có thể kích hoạt hoạt động của CASP, thúc đẩy tình trạng viêm và gây xơ gan. Chức năng quá mức của CASP liên quan đến tình trạng viêm có liên quan trực tiếp đến bệnh nguyên bệnh gan nhiễm mỡ không do rượu , trong đó các phân tử hiệu ứng chính được coi là các cytokine tiền viêm được giải phóng trong khi đó. Hơn nữa, chất nền chung cho CASP gây viêm, GSDMD, hoạt động như một chất trung gian hạ lưu của quá trình hoạt hóa inflammasome không điển hình bằng cách góp phần vào quá trình pyroptosis do CASP gây viêm. Điều quan trọng là, miền GSDMDNT đại diện cho hoạt động gây pyroptosis nội tại ở những bệnh nhân mắc NASH có liên quan tích cực với điểm hoạt động bệnh gan nhiễm mỡ không do rượu và xơ gan. Trên thực tế, gen sinh mỡ Srebp1c điều hòa giảm và điều hòa tăng Pparα , một gen phân giải mỡ, và các mục tiêu hạ lưu của nó, đã tạo ra sự bảo vệ động vật Gsdmd -/- khỏi chứng nhiễm mỡ.
DAMPs và PAMPs có thể gây ra cái chết của tế bào gan liên quan đến pyroptosis trực tiếp hoặc gián tiếp gây tổn thương gan
Như đã đề cập trước đó, DAMPs và PAMPs có thể gây ra cái chết của tế bào gan liên quan đến pyroptosis trực tiếp hoặc gián tiếp gây tổn thương gan. Người ta báo cáo rằng những động vật có đột biến ở Nlrp3 đặc hiệu của dòng tủy không biểu hiện cái chết của tế bào gan qua trung gian pyroptosis có thể phát hiện được và biểu hiện hoạt hóa tế bào gốc tạo máu ít nghiêm trọng hơn. Do đó, người ta có thể kết luận rằng ngoài các tế bào miễn dịch, pyroptosis ở tế bào gan do hoạt hóa inflammasome nội tại có thể làm trầm trọng thêm tình trạng viêm và xơ hóa ở gan, xác định rằng cả hoạt hóa inflammasome NLRP3 đặc hiệu của tế bào miễn dịch và gan đều là những tác nhân thiết yếu gây tổn thương gan. Tuy nhiên, cần phải nghiên cứu những động vật đột biến NLRP3 đặc hiệu của tế bào gan để cung cấp bằng chứng thuyết phục về mối tương quan giữa tế bào gan và pyroptosis trong quá trình khởi phát và tiến triển của tổn thương gan ở bệnh gan nhiễm mỡ không do rượu.
Tài liệu tham khảo
1. Younossi ZM, Golabi P, Paik JM, Henry A, Van Dongen C, Henry L. The global epidemiology of nonalcoholic fatty liver disease (bệnh gan nhiễm mỡ không do rượu ) and nonalcoholic steatohepatitis (NASH): a systematic review. Hepatology. 2023;77:1335-1347
2. Estes C, Razavi H, Loomba R, Younossi Z, Sanyal AJ. Modeling the epidemic of nonalcoholic fatty liver disease demonstrates an exponential increase in burden of disease. Hepatology. 2018;67:123-133.
3. Sun HJ, Jiao B, Wang Y, Zhang YH, Chen G, Wang ZX, Zhao H, Xie Q, Song XH. Necroptosis contributes to non-alcoholic fatty liver disease pathoetiology with promising diagnostic and therapeutic functions. World J Gastroenterol 2024; 30(14): 1968-1981