Bài viết của Dược sĩ Nguyễn Thị Thanh Nga - Dược sĩ Lâm sàng - Khoa Dược - Bệnh viện Đa khoa Quốc tế Vinmec Times City
Vancomycin là kháng sinh glycopeptid đầu tiên được phân lập từ Amycolatopsis orientalis từ giữa những năm 1950. Năm 1958, vancomycin được sử dụng trên lâm sàng để điều trị Staphylococcus aureus kháng penicillin. Tuy nhiên, vài năm sau, kháng sinh này không được ưu tiên dùng nữa do xuất hiện nhiều độc tính do chế phẩm không tinh khiết. Sau khi thay đổi quy trình sản xuất nâng cao độ tinh khiết của chế phẩm, vancomycin lại được sử dụng rộng rãi trở lại từ những năm 1980.
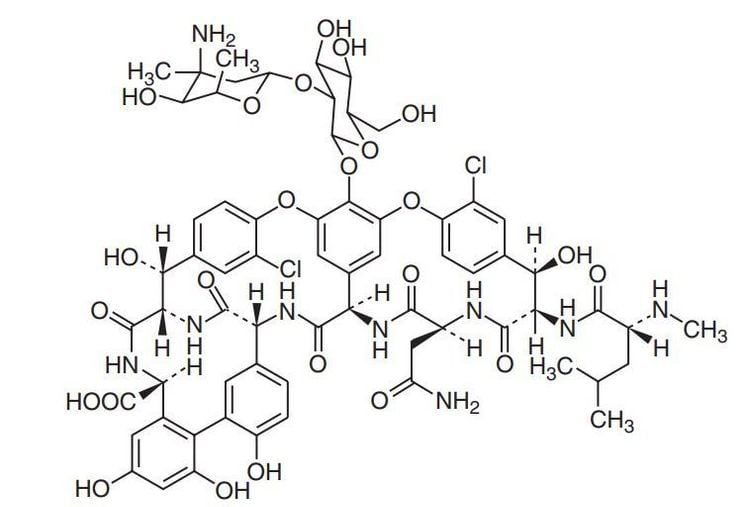
Vancomycin có cấu trúc glycopeptid ba vòng phức tạp gồm 7 chuỗi peptid gắn với disarccharide cấu tạo bởi 2 đường amino (vancosamin và glucose)
1.Mô hình dược động học vancomycin
Sau khi truyền tĩnh mạch trong 1 giờ, nồng độ vancomycin trong máu thường tuân theo mô hình dược động học hai hoặc ba ngăn. Với mô hình hai ngăn, sau khi kết thúc truyền, nồng độ thuốc giảm nhanh do quá trình phân bố từ máu tới các mô (pha α, hay pha phân bố). Sau khoảng 30 – 60 phút của pha phân bố, nồng độ thuốc giảm chậm hơn và tốc độ thải trừ ở pha này là không đổi, phụ thuộc vào chức năng thận (pha β, hay pha thải trừ)
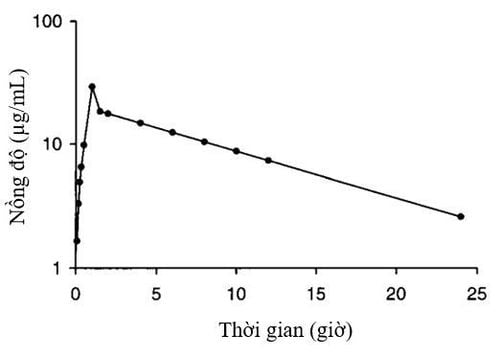
Ở những bệnh nhân có nồng độ vancomycin phân bố theo mô hình ba ngăn, có một pha phân bố trung gian giữa phần α và β của đồ thị. Tuy nhiên, mô hình này khó áp dụng trên lâm sàng do cần xử lý với các công thức toán học phức tạp. Mặt khác, lượng thuốc thải trừ trong thời gian truyền và thời gian đợi kết thúc pha phân bố là không đáng kể. Vì vậy, mô hình dược động học một ngăn đơn giản được sử dụng rộng rãi và cho phép tính liều chính xác khi đo được nồng độ đỉnh (Cpeak) sau pha phân bố. Nồng độ này cần được định lượng sau khi kết thúc truyền 0,5 – 1 giờ.
Các đặc điểm về mô hình được động học của vancomycin chủ yếu dựa trên các nghiên cứu trên người lớn để tìm ra mô hình dược động học của vancomycin trên quần thể bệnh nhân nhi, một số nghiên cứu đã khớp mô hình hai ngăn và đa số các nghiên cứu khác gần đây đều chỉ dùng mô hình dược động học một ngăn để mô tả.
2. Đặc điểm dược động học vancomycin
2.1 Hấp thu
Vancomycin hấp thu rất kém qua đường uống, chỉ dùng trong chỉ định điều trị nhiễm khuẩn đường ruột do Clostridium difficile. Vancomycin dùng đường tiêm bắp gây đau, thậm chí hoại tử vị trí tiêm nên không được khuyên dùng. Vì vậy, thuốc được khuyến cáo dùng đường truyền tĩnh mạch trong điều trị nhiễm khuẩn toàn thân.
2.2 Phân bố
Vancomycin có đặc tính thân nước nên phân bố rộng rãi vào khắp các mô và dịch ngoại bào trong cơ thể, đặc biệt là ở trẻ nhỏ do có tỷ lệ nước trong cơ thể lớn. Ở người lớn không béo phì, thể tích phân bố của vancomycin là 0,7 L/kg (dao động 0,5 – 1 L/kg). Thể tích phân bố (Vd) của vancomycin ở trẻ em dao động giữa các quần thể trong các nghiên cứu khác nhau khoảng 0,636 L/kg ở các bệnh nhân nhi không nằm hồi sức, đến 0,9 L/kg ở bệnh nhân sau mổ tim.
Tỷ lệ liên kết protein huyết tương của vancomycin dao động trong khoảng 30 – 60%. Khả năng thấm qua hàng rào máu não của kháng sinh này rất kém khi màng não không viêm. Ở trẻ em bị viêm màng não, nồng độ thuốc trong dịch não tủy đạt 14% - 28% (trung bình 21%) nồng độ thuốc trong máu sau khi dùng liều 60mg/kg/ngày kết hợp với dexamethason, tỷ lệ này được coi là đủ để diệt khuẩn tại dịch não tủy. Vancomycin có thể thấm tốt vào dịch màng ngoài tim, khoang màng phổi, và các mô dưới da, hoạt dịch, nhưng thấm rất kém vào các mô mỡ [5].
2.3 Chuyển hóa và thải trừ
Vancomycin hầu như không bị chuyển hóa trong cơ thể, khoảng 90% được thải trừ qua thận ở dạng còn hoạt tính nhờ quá trình lọc ở cầu thận. Tốc độ thanh thải vancomycin có tương quan tuyến tính với thanh thải creatinin. Do vậy, liều vancomycin được khuyến cáo hiệu chỉnh dựa vào chức năng thận của từng bệnh nhân. Mặc dù một số nghiên cứu đã báo cáo có sự giảm tốc độ thải trừ của vancomycin trên các bệnh nhân suy giảm chức năng gan, nhưng sự thanh thải thuốc ngoài thận không quá 5%. Vì vậy, việc hiệu chỉnh liều theo chức năng gan là không cần thiết. Mức độ thanh thải và thời gian bán thải thuốc ở trẻ em thay đổi theo lứa tuổi.
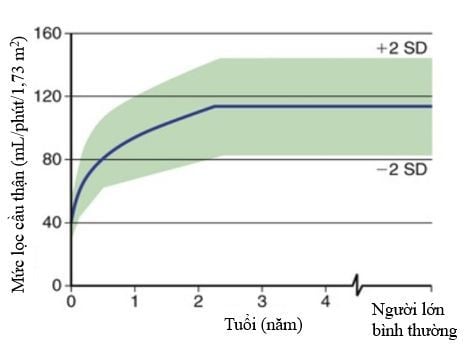
Trẻ sơ sinh có chức năng thận chưa hoàn thiện nên có tốc độ thải trừ thuốc chậm và thời gian bán thải của vancomycin kéo dài, khoảng 5,9 – 9,8 giờ ở trẻ sinh thiếu tháng và khoảng 6,7 giờ ở trẻ sơ sinh đủ tháng. Từ sau 3 tháng tuổi, độ thanh thải vancomycin tăng lên gấp đôi, dẫn tới thời gian bán thải rút ngắn xuống còn khoảng 4 giờ. Mức độ thanh thải vancomyin tiếp tục tăng và thời gian bán thải là 2-3 giờ khi trẻ 4-8 tuổi. Sau giai đoạn này, quá trình thải trừ vancomycin và thời gian bán thải tương tự và đạt giá trị như ở người lớn khi trẻ dậy thì (12-14 tuổi).
3. Đặc điểm dược lực học
3.1 Cơ chế diệt khuẩn
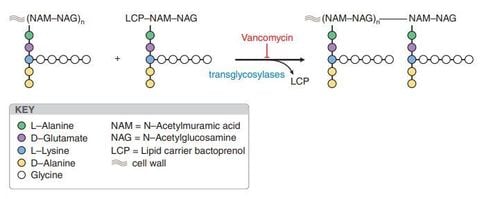
Vancomycin có tác dụng diệt khuẩn thông qua ức chế quá trình sinh tổng hợp vách tế bào vi khuẩn. Do có ái lực liên kết với D-alanyl-D-alanin tận cùng của pentapeptid mới hình thành trong chuỗi peptidoglycan, vancomycin ức chế phản ứng translycosylase ngăn cản sự tạo lưới peptidoglycan, ức chế quá trình tổng hợp vách tế bào. Do cơ chế tác động lên chuỗi peptidoglycan, thuốc không có tác dụng với vi khuẩn Gram âm. Ngoài ra, vancomycin còn tác động đến tính thấm màng tế bào và ức chế quá trình tổng hợp RNA của vi khuẩn.
3.2 Phổ tác dụng
Vancomycin có tác dụng trên nhiều vi khuẩn Gram dương kỵ khí và hiếu khí bao gồm [5]:
- Tụ cầu: Staphylococcus aureus (bao gồm cả các chủng kháng methicillin MRSA), Staphylococcus epidermidis.
- Liên cầu: Streptococcus pneumoniae, S. pyogenes, S. agalactiae, S. bovis, S. mutans.
- Cầu khuẩn ruột: vancomycin có tác dụng kìm khuẩn với phần lớn các chủng Enterococcus faecalis và một tỷ lệ nhất định Enterococcus faecium.
- Clostridium spp.: Vancomycin có tác dụng tốt với hầu hết các chủng bao gồm Clostridium difficile ngoại trừ Clostridium ramosum.
3.3 Cơ chế đề kháng
- Cầu khuẩn ruột Enterococci
Cầu khuẩn ruột Enterococci kháng vancomycin bằng cách thay đổi đích tác dụng D-alanyl-D-alanin thành D-alanyl-D-lactate hoặc D-alanyl - D-serine, làm giảm ái lực với glycopetide, dẫn đến giảm sự ức chế tổng hợp peptidoglycan. Đề kháng glycopeptid thường gặp nhất ở E. faecium (khoảng 80%), sau đó là E. faecalis (khoảng 5%) và ít gặp ở các cầu khuẩn đường ruột khác.
- Tụ cầu vàng (Staphylococcus aureus)
Cơ chế đề kháng của tụ cầu vàng với vancomycin chính là sự dày lên của thành tế bào vi khuẩn (vi khuẩn tăng cường tổng hợp D-alanyl-D-alanin, tạo ra các đích giả cho vancomycin do đó làm giảm tác dụng của vancomycin). Nhờ cơ chế đó, hiện nay đã xuất hiện các chủng tụ cầu vàng đề kháng trung gian với vancomycin (VISA - Vancomycin intermediate Staphylococcus aureus), tụ cầu vàng dị đề kháng vancomycin (hVISA - hetero Vancomycin intermediate Staphylococcus aureus), và tụ cầu vàng kháng vancomycin (VRSA - vancomycin resistance Staphylococcus aureus).
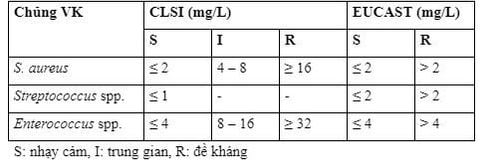
Mức độ nhạy cảm của các vi khuẩn với vancomycin thể hiện bằng thông số nồng độ ức chế tối thiểu (MIC). Điểm gãy nhạy cảm của vancomycin được quy định bởi Viện chuẩn hóa lâm sàng và xét nghiệm Mỹ (CLSI) và Ủy ban thử nghiệm độ nhạy cảm kháng sinh Châu Âu (EUCAST) được trình bày tại bảng.
Trên đây là những thông tin quan trọng về kháng sinh vancomycin. Việc hiểu rõ về thuốc sẽ giúp người bệnh nắm rõ hơn về công dụng và những vấn đề gặp phải khi dùng.
Để đặt lịch khám tại viện, Quý khách vui lòng bấm số HOTLINE hoặc đặt lịch trực tiếp TẠI ĐÂY. Tải và đặt lịch khám tự động trên ứng dụng MyVinmec để quản lý, theo dõi lịch và đặt hẹn mọi lúc mọi nơi ngay trên ứng dụng.
Nguồn tham khảo:
- McEvoy Gerald K, Snow Elaine K (2019), AHFS Drug Information (2019), American Society of Health-System Pharmacists, pp.
- Moffett Brady S, Resendiz Karla, et al. (2019), "Population pharmacokinetics of vancomycin in the pediatric cardiac surgical population", The Journal of Pediatric Pharmacology and Therapeutics, 24(2), pp. 107-116.
- Bauer L. A., Black D. J., et al. (1998), "Vancomycin dosing in morbidly obese patients", Eur J Clin Pharmacol, 54(8), pp. 621-5.
- Bauer Larry A (2008), Applied clinical pharmacokinetics, pp. 207 - 296.
- Bennett John E, Dolin Raphael, et al. (2015), Mandell, douglas, and bennett's principles and practice of infectious diseases, Elsevier Health Sciences, pp. 377-388.
- Blouin R. A., Bauer L. A., et al. (1982), "Vancomycin pharmacokinetics in normal and morbidly obese subjects", Antimicrob Agents Chemother, 21(4), pp. 575-80.
- Brunton L L Hilal-Dandan R, et al (2017), "Goodman and Gilman's The Pharmacological Basis of Therapeutics," pp. 1059 - 1061.
- Clinical and LaboratoryStandards Institute (2019), Performance standards for Antimicrobial Sucepcibility Testing, M100, pp. 1-25.
- Lamarre Patrice, Lebel Denis, et al. (2000), "A Population Pharmacokinetic Model for Vancomycin in Pediatric Patients and Its Predictive Value in a Naive Population", Antimicrobial Agents and Chemotherapy, 44(2), pp. 278.
- Le J., Vaida F., et al. (2014), "Population-Based Pharmacokinetic Modeling of Vancomycin in Children with Renal Insufficiency", J Pharmacol Clin Toxicol, 2(1), pp. 1017-1026.
- Le Jennifer, Bradley John S, et al. (2013), "Improved vancomycin dosing in children using area-under-the-curve exposure", The Pediatric infectious disease journal, 32(4), pp. e155.
- Lietman Paul S, Schaad Urs B, et al. (1980), "Clinical pharmacology and efficacy of vancomycin in pediatric patients", The Journal of pediatrics, 96(1), pp. 119-126.
- Matzke G. R., Kovarik J. M., et al. (1985), "Evaluation of the vancomycin-clearance:creatinine-clearance relationship for predicting vancomycin dosage", Clin Pharm, 4(3), pp. 311-5.
- Moellering R. C., Jr., Krogstad D. J., et al. (1981), "Vancomycin therapy in patients with impaired renal function: a nomogram for dosage", Ann Intern Med, 94(3), pp. 343-6.
- Mulla H., Pooboni S. (2005), "Population pharmacokinetics of vancomycin in patients receiving extracorporeal membrane oxygenation", Br J Clin Pharmacol, 60(3), pp. 265-75.
- Stockmann C., Olson J., et al. (2019), "An Evaluation of Vancomycin Area Under the Curve Estimation Methods for Children Treated for Acute Pulmonary Exacerbations of Cystic Fibrosis Due to Methicillin-Resistant Staphylococcus aureus", J Clin Pharmacol, 59(2), pp. 198-205.
- N ang Y., Gao P., et al. (2019), "How Much Vancomycin Dose Is Enough For The MRSA Infection in Pediatric Patients With Various Degrees of Renal Function?", Iran J Pharm Res, 18(2), pp. 995-1009. N