Bài viết bởi Thạc sĩ, Bác sĩ Mai Viễn Phương - Bác sĩ nội soi tiêu hóa - Khoa Khám bệnh & Nội khoa - Bệnh viện Đa khoa Quốc tế Vinmec Central Park
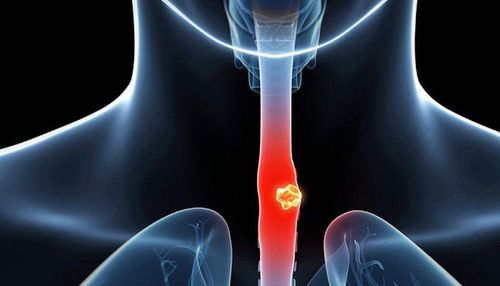
Do diễn tiến nhanh và tiên lượng xấu của ung thư thực quản (EC) nên việc phát hiện và chẩn đoán sớm ung thư thực quản sớm có giá trị rất lớn trong việc cải thiện tiên lượng cho bệnh nhân. Hiện nay, khoa học đã ứng dụng trí tuệ nhân tạo trong phương pháp soi nội bào chẩn đoán ung thư sớm thực quản.
Chữ viết tắt:
EC: Ung thư thực quản
AI: artificial intelligence
BE: Barrett thực quản
1. Trí tuệ nhân tạo là gì?
Trí tuệ nhân tạo (AI: Artificial Intelligence) có thể được định nghĩa như một ngành của khoa học máy tính liên quan đến việc tự động hóa các hành vi thông minh. AI là một bộ phận của khoa học máy tính và do đó nó phải được đặt trên những nguyên lý lý thuyết vững chắc, có khả năng ứng dụng được của lĩnh vực này.

2. Tổng quan về ứng dụng của trí tuệ nhân tạo với nội soi tiêu hoá
Do diễn tiến nhanh và tiên lượng xấu của ung thư thực quản (EC) nên việc phát hiện và chẩn đoán sớm ung thư thực quản có giá trị rất lớn trong việc cải thiện tiên lượng cho bệnh nhân. Tuy nhiên, nội soi phát hiện sớm ung thư thực quản, đặc biệt là loạn sản Barrett hoặc loạn sản biểu mô vảy thực quản rất khó. Do đó, yêu cầu về các phương pháp phát hiện các đặc điểm ung thư thực quản sớm hiệu quả hơn đã dẫn đến các nghiên cứu chuyên sâu trong lĩnh vực trí tuệ nhân tạo (AI). Kỹ thuật học và ghi nhớ - Deep learing (DL) đã mang lại những đột phá trong việc xử lý hình ảnh, video và các khía cạnh khác, trong khi hệ thống mạng nơ-ron phức tạp (CNN) đã mở đường cho việc phát hiện hình ảnh và video nội soi có độ phân giải cao.
3. Giới thiệu về ung thư thực quản
Ung thư thực quản (EC) là bệnh ung thư phổ biến thứ tám và là nguyên nhân gây tử vong do ung thư đứng hàng thứ sáu trên toàn thế giới. Ung thư thực quản chủ yếu bao gồm ung thư biểu mô tuyến thực quản (EAC) và ung thư biểu mô tế bào vảy thực quản (ESCC). Ung thư biểu mô tuyến thực quản là loại bệnh lý phổ biến nhất ở các nước phương Tây, hơn 40% bệnh nhân mắc ung thư biểu mô tuyến thực quản được chẩn đoán sau khi bệnh đã di căn và tỷ lệ sống 5 năm dưới 20%.
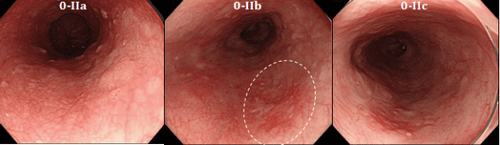
Mặc dù tỷ lệ mắc ung thư biểu mô tuyến thực quản đang gia tăng trên toàn cầu, ung thư biểu mô tế bào vảy thực quản vẫn là loại bệnh lý phổ biến nhất (80%) trong số tất cả các ung thư thực quản với tỷ lệ mắc bệnh cao nhất trên “vành đai ung thư” kéo dài từ Đông Phi và qua Trung Đông đến châu Á. Chỉ 20% bệnh nhân ung thư biểu mô tế bào vảy thực quản sống sót lâu hơn 3 năm, chủ yếu do chẩn đoán giai đoạn muộn. Ở những nơi có nguồn tài nguyên thấp, tỷ lệ sống sót sau 5 năm thấp hơn nhiều vào khoảng 3,4%. Chẩn đoán sớm có thể giúp cải thiện đáng kể kết quả cho tất cả các ung thư thực quản.
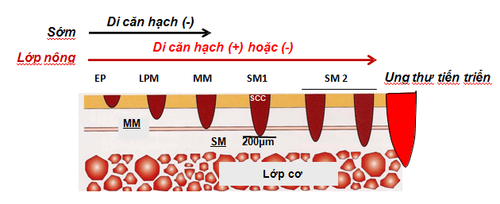
4. Vai trò của trí tuệ nhân tạo AI trong phát hiện sớm ung thư thực quản
4.1. Chứng loạn sản Barrett và ung thư biểu mô tuyến thực quản giai đoạn sớm
Trí tuệ nhân tạo AI dựa trên hệ thống nội soi ánh sáng trắng (WLE) và hệ thống nội soi dải tần số hẹp NBI: Có một số hạn chế để nhận ra các tổn thương ung thư sớm liên quan đến Barrett thực quản bằng WLE, một công nghệ thông thường. WLE độ nét cao (HD-WLE) và hệ thống nội soi NBI đã từng được coi là để nâng cao độ chính xác của việc chẩn đoán các tổn thương ung thư sớm liên quan đến Barrett thực quản. Nhưng sự cải tiến vẫn chưa làm hài lòng các bác sĩ nội soi. Tình huống này đã kích thích sự phát triển của hệ thống CAD cho các tổn thương ung thư sớm ở Barrett thực quản dựa trên thuật toán học máu ML được giám sát. Tuy nhiên, hệ thống này vẫn gặp khó khăn trong việc xác định các tổn thương ung thư sớm liên quan đến Barrett thực quản và chọn các vị trí sinh thiết. Độ chính xác của hệ thống sử dụng HD-WLE tốt hơn so với hệ thống nội soi nói chung. Hơn nữa, hệ thống hiển thị khả năng xác định vị trí tổn thương và tỷ lệ trùng khớp vùng giữa các tổn thương do hệ thống và các chuyên gia khoanh vùng lên đến 72%. Nói chung, độ đặc hiệu của NBI cao hơn so với WLE thông thường. So với việc sử dụng HD-WLE, hệ thống không có lợi thế rõ ràng khi sử dụng hệ thống NBI.
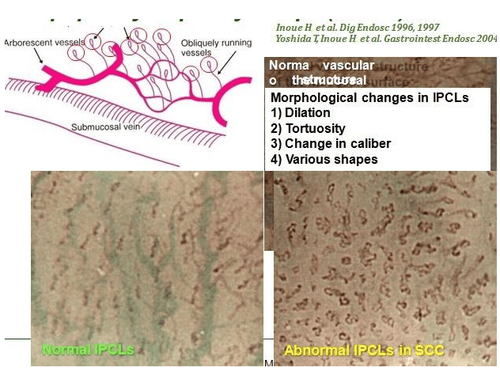
5. Vai trò của chụp cắt lớp quang kết hợp qua nội soi (EOCT) và nội soi bằng laser đồng tiêu (CLE)
Trí tuệ nhân tạo AI dựa trên chụp cắt lớp quang học nội soi và nội soi bằng laser đồng tiêu: Ngoài WLE và NBI, kỹ thuật chụp cắt lớp quang kết hợp qua nội soi (EOCT) và nội soi bằng laser đồng tiêu (CLE) cũng được sử dụng để chẩn đoán sớm chứng loạn sản liên quan đến EAC / BE. EOCT có thể xác định các tổn thương khối u sớm liên quan đến Barrett thực quản bằng cách phân tích các cấu trúc niêm mạc và dưới niêm mạc thực quản. CLE có thể quan sát mô niêm mạc và hình thái tế bào để đạt được sinh thiết quang học. Tuy nhiên, sự phức tạp của hai công nghệ hình ảnh này, việc đọc hình ảnh mất nhiều thời gian và yêu cầu bác sĩ nội soi cao cấp đã hạn chế việc sử dụng chúng trên lâm sàng. Để giải quyết vấn đề này, Qi và cộng sự đã trích xuất nhiều đặc điểm hình ảnh EOCT và kết hợp một hoặc nhiều đặc điểm để phân loại tổn thương, nhưng kết quả không khả quan. Sau đó, Swager và cộng sự đã sử dụng hình ảnh nội soi bằng laser thể tích (VLE, tích hợp với OCT thế hệ thứ hai) để đào tạo và thử nghiệm, và kết quả cho thấy hệ thống CAD vượt trội hơn so với các chuyên gia VLE. Veronese và cộng sự đã sử dụng hình ảnh CLE, và kết quả cho thấy hệ thống có thể phân biệt chính xác chuyển sản dạ dày (GM), chuyển sản ruột (IM) và tân sinh. Ghatwary và cộng sự cho thấy độ nhạy của hệ thống sử dụng hình ảnh CLE để chẩn đoán IM và ung thư cao hơn đáng kể so với hệ thống để chẩn đoán GM. Tương tự, hệ thống CAD do Hong thiết lập đã không xác định được GM, độ nhạy chẩn đoán IM không khác biệt đáng kể so với nghiên cứu trên và độ nhạy chẩn đoán ung thư cũng giảm nhẹ. Điều này có thể là do số lượng hình ảnh GM và tân sinh có hạn. Hiện tại, có rất ít nghiên cứu lâm sàng trong lĩnh vực này và hình ảnh có sẵn còn hạn chế. Trong tương lai, cần có thêm nhiều nghiên cứu để khẳng định giá trị của VLE / CLE kết hợp với trí tuệ nhân tạo AI trong chẩn đoán sớm EAC.
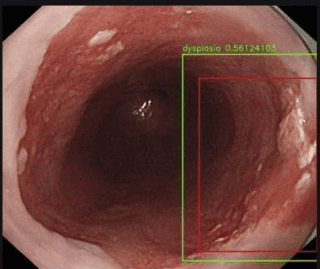
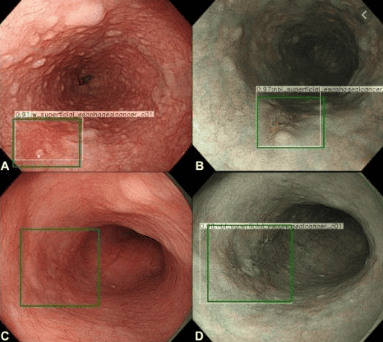
6. Vai trò của trí tuệ nhân tạo AI trong phương pháp soi nội bào (nội soi ở mức độ tế bào)
Trí tuệ nhân tạo AI dựa trên phương pháp soi nội bào và nội soi vi mô độ phân giải cao: Nội soi nội bào (nội soi ở mức độ tế bào) là một công nghệ mới kết hợp nội soi phóng đại với phương pháp nhuộm quan trọng. Do khả năng phóng đại tuyệt vời nên người nội soi có thể quan sát rõ các tế bào biểu mô của niêm mạc thực quản để đạt được hiệu quả tương tự như chẩn đoán bệnh lý. Tuy nhiên, nếu các bác sĩ nội soi muốn sử dụng nội soi để hoàn thành việc phát hiện thời gian thực một cách độc lập, họ cần một nền tảng vững chắc về bệnh lý, điều này rõ ràng là không thực tế. Do đó, AI có thể là lựa chọn tốt để hỗ trợ chẩn đoán nội soi. Kumagai và cộng sự đã chỉ ra rằng hiệu suất của hệ thống sử dụng ảnh có độ phóng đại cao hơn tốt hơn so với hệ thống sử dụng ảnh có độ phóng đại thấp hơn. Tuy nhiên, không có phân tích phân tầng ung thư thực quản nông và ung thư thực quản tiến triển trong nghiên cứu này. Kết quả không thể phản ánh chính xác khả năng của nội soi kết hợp với AI trong chẩn đoán ung thư thực quản sớm. Kính hiển vi có độ phân giải cao (HRME) có thể được sử dụng để quan sát mô niêm mạc thực quản và hình thái tế bào. Shin và cộng sự đã thử nghiệm khả năng của các đặc điểm hình ảnh khác nhau để phân biệt khối u với các tổn thương không phải khối u, và các đặc điểm tốt được chọn có độ nhạy 84% và độ đặc hiệu 95%. Tuy nhiên, phải mất nhiều thời gian để phân tích một hình ảnh và độ nhạy không lý tưởng. Trong tương lai, cần có thêm nhiều nghiên cứu chất lượng cao để khẳng định vai trò của nó trong chẩn đoán ung thư thực quản sớm.
6.1. Chẩn đoán qua nội soi theo thời gian thực bằng AI
Quang và cộng sự sử dụng dữ liệu hình ảnh HRME giống như Shin và cộng sự để đào tạo và xác nhận, kết quả cho thấy độ nhạy là 95% và độ đặc hiệu là 91% trong chẩn đoán ung thư thực quản sớm. Sau đó, ba bệnh nhân nghi ngờ ung thư thực quản được kiểm tra nội soi với độ chính xác 100%. Tuy nhiên, có một số hạn chế trong nghiên cứu này.
- Thứ nhất, số lượng bệnh nhân và hình ảnh trong chẩn đoán thời gian thực quá ít.
- Thứ hai, hệ thống vẫn sử dụng hình ảnh để chẩn đoán, không phải video để phát hiện thời gian thực.
Everson, cộng sự và Guo, cộng sự đã thiết lập hệ thống CAD dựa trên DL với hiệu suất chẩn đoán tốt bằng cách sử dụng video dải tần hẹp NBI. Thật không may, các hệ thống này đã không được áp dụng trong chẩn đoán thời gian thực.
6.2. Vai trò của AI trong chẩn đoán mô bệnh học của ung thư sớm thực quản
Mặc dù AI kết hợp chẩn đoán nội soi đã có nhiều tiến bộ nhưng chẩn đoán nội soi vẫn không thể thay thế tiêu chuẩn vàng trong chẩn đoán bệnh lý. Tuy nhiên, có một vấn đề trong việc chẩn đoán bệnh lý của tân sinh thực quản sớm, nghĩa là, độ chính xác của việc chẩn đoán loạn sản không phải là lý tưởng với sự thay đổi đáng kể giữa máy chủ quan sát. Để giải quyết vấn đề này, Sabo và cộng sự đã thiết lập hai mô hình để phân biệt không loạn sản (ND) với loạn sản cấp thấp (LGD) và LGD từ loạn sản cấp cao (HGD) bằng cách trích xuất hình ảnh phần bệnh lý nhuộm màu hematoxylin và eosin (HE). Đặc điểm của bệnh nhân Barrett thực quản BE. Kết quả cho thấy hai mô hình thực hiện tốt trong chẩn đoán tổn thương đường viền không phân biệt được. Baak và cộng sự đã kết hợp các đặc điểm hình ảnh mặt cắt bệnh lý nhuộm HE với các chỉ số hóa mô miễn dịch p53 / Ki67 và sử dụng các mẫu bệnh phẩm của phẫu thuật cắt bỏ quan nội soi tiêu hoá và mẫu sinh thiết nội soi của Barrett thực quản để xét nghiệm. Người ta thấy rằng hệ thống hoạt động tốt trong việc phân biệt ND từ LGD và LGD với HGD. Tuy nhiên, độ chính xác của việc phân biệt HGD với ung thư biểu mô trong niêm mạc cần được cải thiện. Hiệu suất của hệ thống tốt hơn so với của bác sĩ bệnh lý nói chung và chỉ kém hơn một chút so với bác sĩ bệnh lý có kinh nghiệm.
6.3. Vai trò của trí tuệ nhân tạo AI trong phân tầng nguy cơ của ung thư sớm thực quản
Người ta đánh giá rằng chỉ 0,12% -0,43% bệnh nhân Barrett thực quản có thể tiến triển thành ung thư thực quản sớm mỗi năm, đặc biệt cần thiết phải thiết lập một mô hình hiệu quả để dự đoán nguy cơ ung thư thực quản sớm mỗi năm ở bệnh nhân Barrett thực quản. Sự phân tầng nguy cơ trước đây chủ yếu dựa trên sự hiện diện của chứng loạn sản, nhưng hiệu quả của nó không lý tưởng. Critchley-Thorne và cộng sự đã thiết lập một mô hình dự đoán dựa trên sự khác biệt đặc trưng của các dấu hiệu miễn dịch mô huỳnh quang và hình ảnh mô bệnh học, cụ thể giữa bệnh nhân Barrett thực quản đã phát triển ung thư thực quản sớm mỗi năm và những người không mắc bệnh. Kết quả không khả quan, với hơn 30% bệnh nhân Barrett thực quản phát triển ung thư thực quản sớm mỗi năm được phân loại là nguy cơ thấp.
Trí tuệ nhân tạo AI đang cố gắng được sử dụng để phát hiện nội soi, chẩn đoán bệnh lý, chẩn đoán gen và dự đoán nguy cơ ung thư của ung thư thực quản sớm. Nó rất hữu ích cho các bác sĩ nội soi và bác sĩ giải phẫu bệnh để cải thiện độ chính xác của chẩn đoán và hỗ trợ bác sĩ điều trị và đưa ra các chiến lược tiếp theo.
Hiện nay, khám sàng lọc ung thư đường tiêu hoá là biện pháp khoa học và hiệu quả để phát hiện sớm ung thư đường tiêu hóa (ung thư thực quản, ung thư dạ dày, ung thư đại tràng) và đưa ra phác đồ điều trị tốt. Hiện tại, Bệnh viện Đa khoa Quốc tế Vinmec có Gói tầm soát và phát hiện sớm ung thư đường tiêu hóa (thực quản - dạ dày - đại tràng) kết hợp khám lâm sàng và cận lâm sàng để đem lại kết quả chính xác nhất có thể.
Khi sàng lọc ung thư đường tiêu hóa tại Vinmec, Quý khách sẽ được:
- Khám Chuyên khoa Nội tiêu hóa với bác sĩ chuyên khoa ung bướu (có hẹn).
- Nội soi dạ dày và nội soi đại tràng với máy nội soi NBI có gây mê.
- Xét nghiệm tổng phân tích tế bào máu ngoại vi (bằng máy đếm laser).
- Xét nghiệm thời gian prothrombin bằng máy tự động.
- Xét nghiệm thời gian thrombin bằng máy tự động.
- Xét nghiệm thời gian thromboplastin một phần hoạt hoá (APTT: Activated Partial Thromboplastin Time) bằng máy tự động.
- Siêu âm ổ bụng tổng quát
Để đặt lịch khám tại viện, Quý khách vui lòng bấm số HOTLINE hoặc đặt lịch trực tiếp TẠI ĐÂY. Tải và đặt lịch khám tự động trên ứng dụng MyVinmec để quản lý, theo dõi lịch và đặt hẹn mọi lúc mọi nơi ngay trên ứng dụng.
Tài liệu tham khảo
- Bray F, Ferlay J, Soerjomataram I, Siegel RL, Torre LA, Jemal A. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2018;68:394-424. [PubMed] [DOI]
- Hur C, Miller M, Kong CY, Dowling EC, Nattinger KJ, Dunn M, Feuer EJ. Trends in esophageal adenocarcinoma incidence and mortality. Cancer. 2013;119:1149-1158. [PubMed] [DOI]
- Thrift AP. The epidemic of oesophageal carcinoma: Where are we now? Cancer Epidemiol. 2016;41:88-95. [PubMed] [DOI]
- Lu-Ming Huang, Wen-Juan Yang, Zhi-Yin Huang, Cheng-Wei Tang, Jing Li, Artificial intelligence technique in detection of early esophageal cancer, World J Gastroenterol. Oct 21, 2020; 26(39): 5959-5969