Thuốc được sử dụng rộng rãi để điều trị các bệnh khác nhau trong y học hiện đại, nhưng chúng thường đi kèm với các tác dụng phụ. Những tác dụng phụ nằm ở đường tiêu hóa thường gặp và thường nhẹ, nhưng chúng có thể nghiêm trọng hoặc đe dọa tính mạng và quyết định việc tiếp tục điều trị.
Bài viết được viết bởi ThS. BS Mai Viễn Phương - Trưởng đơn nguyên Nội soi tiêu hóa - Khoa Khám bệnh & Nội khoa - Bệnh viện Đa khoa Quốc tế Vinmec Central Park.
Dạ dày thường bị ảnh hưởng không chỉ bởi thuốc uống mà còn bởi thuốc tiêm. Ở đây, chúng tôi xem xét các cơ chế gây tổn thương, các yếu tố nguy cơ và các đặc điểm nội soi, mô bệnh học và lâm sàng cụ thể của những loại thuốc thường liên quan đến tổn thương dạ dày, cụ thể là NSAID, aspirin, thuốc chống đông máu, glucocorticosteroid, thuốc chống ung thư, chế phẩm sắt uống và thuốc ức chế bơm proton.
Thuốc chống viêm không steroid/Axit acetylsalicylic (NSAID/Aspirin)
Mô tả đầu tiên về hình ảnh nội soi về tổn thương niêm mạc dạ dày liên quan đến việc sử dụng aspirin đã được A. Douthwait và J. Lintoff công bố vào năm 1938.
Dịch tễ học
NSAID là một trong những nhóm thuốc được kê đơn phổ biến nhất với nhiều chỉ định và tính khả dụng ở dạng không kê đơn. Theo một số nghiên cứu, tỷ lệ sử dụng NSAID và aspirin ở người lớn tuổi là 24,7%. Xói mòn dạ dày xảy ra ở khoảng một nửa số bệnh nhân dùng NSAID và bệnh loét dạ dày tá tràng xảy ra ở 15–30% các trường hợp. Loét dạ dày tá tràng có triệu chứng có thể được quan sát thấy ở 3–4,5% bệnh nhân dùng NSAID và các biến chứng nghiêm trọng (thủng, tắc nghẽn hoặc chảy máu) xảy ra ở khoảng 1,5% bệnh nhân sau 1 năm điều trị.
Theo dữ liệu từ Tây Ban Nha, tỷ lệ tử vong liên quan đến việc sử dụng NSAID hoặc aspirin là 5,6%, tương đương với 15,3 trường hợp tử vong trên 100.000 người dung.
Các yếu tố rủi ro
Các yếu tố nguy cơ phát triển bệnh lý dạ dày liên quan đến NSAID/aspirin bao gồm những người trên 60 tuổi (và đặc biệt là những người trên 70 tuổi), điều trị bằng NSAID liều cao, tiền sử loét dạ dày tá tràng có hoặc không có biến chứng, điều trị đồng thời bằng aspirin liều thấp, thuốc chống đông máu, thuốc ức chế tái hấp thu serotonin hoặc steroid và nhiễm trùng H. pylori.
Cơ chế gây tổn thương dạ dày
Tổn thương do NSAID/aspirin liên quan đến đường tiêu hóa dựa trên sự phong tỏa enzyme cyclooxygenase (COX), enzyme này điều hòa quá trình tổng hợp prostaglandin từ axit arachidonic. COX tồn tại dưới hai dạng đồng phân: COX-1 cấu trúc và COX-2 cảm ứng. Dạng đồng phân COX-2 không được phát hiện trong các mô bình thường. Sự biểu hiện của nó được kích thích bởi các chất trung gian gây viêm (lipopolysaccharides, interleukin-1, yếu tố hoại tử khối u alpha, đại thực bào, bạch cầu đơn nhân) và gây ra tất cả các biểu hiện lâm sàng của quá trình viêm: đau nhức, sốt, sưng và rối loạn chức năng. Do đó, chính sự phong tỏa COX-2 gây ra các tác dụng dược lý mục tiêu chính của NSAID/aspirin, bao gồm chống viêm, giảm đau và hạ sốt. Đồng thời, sự phong tỏa COX-1 gây ra sự giảm toàn thân trong quá trình tổng hợp prostaglandin (PG), có tác dụng bảo vệ tế bào.
Người ta đã xác định rằng PGE2 ức chế sự hình thành ion H+ và pepsinogen trong dạ dày, làm giảm thể tích tiết dịch vị và hoạt động của axit và peptic; tuy nhiên, tác dụng chính là làm tăng sản xuất chất nhầy và bicarbonate, kích thích quá trình tăng sinh tế bào và tái tạo sinh lý của các tế bào biểu mô niêm mạc dạ dày. Do đó, việc giảm tổng hợp PG có liên quan đến việc giảm sức đề kháng của niêm mạc dạ dày, cũng như làm giảm lưu lượng máu đến niêm mạc dạ dày do khả năng của NSAID/aspirin ức chế tổng hợp nitric oxide (NO) thông qua việc ức chế hoạt động của enzym NO synthetase. Đồng thời, sự giảm hình thành PG dẫn đến hoạt hóa con đường lipoxygenase, với sự gia tăng tổng hợp leukotrienes (LTs), chủ yếu là LT-B4 và các cytokine tiền viêm (C5-compliment, yếu tố hoại tử khối u-α), làm trầm trọng thêm tình trạng viêm và thiếu máu cục bộ của niêm mạc dạ dày.
Tương tác trực tiếp (tại chỗ) giữa NSAID và phospholipid và sự tách rời của quá trình phosphoryl hóa oxy hóa trong ty thể gây ra tổn thương màng tế bào, với sự phá vỡ lớp phospholipid và các mối nối chặt. Tác động này làm tăng tính thấm xuyên tế bào. Sự ức chế COX, như một tác dụng toàn thân, làm giảm lưu lượng máu vi mạch và các yếu tố gây hấn trong lòng ống làm thay đổi và khuếch đại phản ứng này, dẫn đến viêm, xói mòn và loét.
Tùy thuộc vào khả năng phong tỏa một dạng đồng phân COX này hay dạng khác, NSAID được chia thành loại chọn lọc (chỉ ức chế COX-2) và loại không chọn lọc (ức chế cả COX-1 và COX-2). Thuốc chọn lọc, được gọi là “coxib”, có tác dụng ít gây hại hơn đối với niêm mạc dạ dày và tá tràng và ban đầu được sử dụng để ngăn ngừa tổn thương đường tiêu hóa liên quan đến NSAID. Tuy nhiên, sau đó người ta phát hiện ra rằng khi nguy cơ đường tiêu hóa giảm khi dùng NSAID chọn lọc, nguy cơ mắc các biến cố tim mạch gây tử vong sẽ tăng lên. Xem xét DIG, chúng ta cũng nên lưu ý rằng tác dụng gây hại của những loại thuốc này có thể được nhận thấy trên toàn bộ đường tiêu hóa và tiến triển với nhận thức về sự liên quan của các cơ quan và hệ thống khác (gan, thận, v.v.).
Cơ chế phát triển bệnh lý dạ dày liên quan đến NSAID được thể hiện ở Hình 1 .
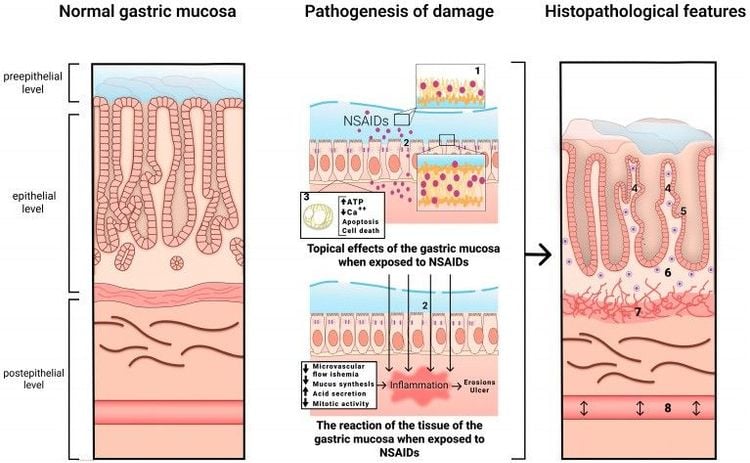
Biểu hiện lâm sàng
Theo nguyên tắc, hầu hết bệnh nhân dùng NSAID không có triệu chứng đường tiêu hóa. Tuy nhiên, các triệu chứng khó tiêu có thể xảy ra ở một số lượng lớn bệnh nhân, bao gồm đau thượng vị (17–20%) và buồn nôn (22%). Trong một số trường hợp, có thể có các triệu chứng như ợ nóng, ợ chua, táo bón (19,3%) hoặc tiêu chảy (9,2%) cho thấy các bộ phận khác của đường tiêu hóa có liên quan.
Một đặc điểm hiếm gặp nhưng quan trọng về mặt lâm sàng của bệnh lý dạ dày liên quan đến NSAID/aspirin là sự phát triển của các biến chứng, chủ yếu là chảy máu đường tiêu hóa với nguy cơ chảy máu cao nhất trong 3 tháng đầu tiên dùng NSAID (OR 11,7; 6,5–21,0) và giảm dần khi tiếp tục sử dụng, trở nên tối thiểu sau 1 tuần ngừng thuốc (OR 3,2; 2,1–5,1). Tỷ lệ tuyệt đối chảy máu loét dạ dày tá tràng ở những bệnh nhân dùng các hợp chất này được báo cáo là 1% mỗi năm, nhưng tỷ lệ này có thể tăng đáng kể ở những bệnh nhân có các yếu tố nguy cơ như tuổi cao, tiền sử loét dạ dày tá tràng và sử dụng đồng thời các thuốc khác, chẳng hạn như thuốc chống đông máu, thuốc chống tiểu cầu, corticosteroid và thuốc ức chế tái hấp thu serotonin. Loét chảy máu có thể được chỉ ra bằng sự xuất hiện của nôn ra máu và/hoặc phân đen, nhưng một số bệnh nhân có thể chỉ báo cáo các triệu chứng chung của mất máu như giảm huyết áp, nhịp tim nhanh, da nhợt nhạt, chóng mặt hoặc thiếu máu. Một số bệnh nhân bị bệnh dạ dày do NSAID/aspirin có thể không có triệu chứng.
Điều quan trọng cần lưu ý là tổn thương đường tiêu hóa khi dùng NSAID/aspirin không chỉ giới hạn ở niêm mạc dạ dày và tá tràng mà còn có thể ảnh hưởng đến ruột non và ruột già, như đã được chứng minh trong một số thử nghiệm lâm sàng ngẫu nhiên quy mô lớn. Thông thường, tổn thương liên quan đến NSAID/aspirin ở đường tiêu hóa dưới đi kèm với mất máu tiềm ẩn và phát triển tình trạng thiếu máu do thiếu sắt mãn tính, làm trầm trọng thêm quá trình bệnh tim mạch và bệnh lý phế quản phổi và làm tăng nguy cơ biến chứng huyết khối tắc mạch. Bệnh lý ruột liên quan đến NSAID/aspirin đi kèm, ngoài tình trạng thiếu sắt, còn là mất protein và giảm albumin máu. Một dấu hiệu bệnh lý đặc trưng của tổn thương ruột non (hiếm khi là ruột già), liên quan đến việc sử dụng NSAID trong thời gian dài, là hình thành các hẹp tròn giống cơ hoành do quá trình viêm mãn tính, có thể gây tắc ruột.
Hình ảnh nội soi
Vị trí điển hình của các tổn thương loét và xói mòn niêm mạc là hang vị dạ dày, nhưng tất cả các vùng của đường tiêu hóa từ dạ dày đến tá tràng đều có thể bị ảnh hưởng. Tình trạng này được đặc trưng bởi tổn thương có bản chất đa dạng, có thể là cấp tính và mãn tính. Các dấu hiệu chảy máu và xuất huyết dưới biểu mô thường được ghi nhận. Trong quá trình chữa lành vết loét, theo quy luật, các vết sẹo thô và biến dạng không hình thành, niêm mạc hầu như trở về bình thường.
Kiểm tra mô học
Các dấu hiệu vi thể bao gồm hình ảnh của cái gọi là bệnh lý dạ dày phản ứng, không hoàn toàn đặc hiệu với NSAID. Có một sự thâm nhiễm viêm yếu-lan tỏa, chủ yếu là đơn nhân của lớp niêm mạc, thường biểu hiện các khiếm khuyết xói mòn và/hoặc loét, những thay đổi tái tạo rõ rệt ở biểu mô (tăng sản nang với nhân tế bào tăng sắc tố, giảm hình thành chất nhầy), phù niêm mạc với giãn mạch máu ở lớp niêm mạc và sự giãn nở của lớp niêm mạc với sự tăng sinh xơ cơ. Các tế bào niêm mạc có không bào dưới nhân có thể là một tiêu chuẩn bổ sung, liên quan đến hội chứng dạ dày đã phẫu thuật.
Điều thú vị là bản chất của các khối hoại tử ở dưới cùng của khiếm khuyết có thể là điểm khởi đầu cho chẩn đoán phân biệt giữa các tổn thương liên quan đến NSAID với vùng khối hoại tử ái toan đồng nhất và khiếm khuyết do Helicobacter pylori ( H. pylori ) gây ra với sự hiện diện của các khối hoại tử liên kết lỏng lẻo với lớp niêm mạc, với các mảnh bị che khuất, tế bào hoại tử và bạch cầu trung tính ( Hình 2 ). Trong những trường hợp rất hiếm, phơi nhiễm NSAID đi kèm với sự hình thành cơ hoành (bệnh cơ hoành) trong dạ dày. Hiện tượng này điển hình hơn đối với tổn thương ở ruột non và ruột già.
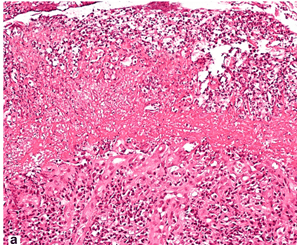
Tài liệu tham khảo
1. Hill C, Guarner F, Reid G, Gibson GR, Merenstein DJ, Pot B, Morelli L, Canani RB, Flint HJ, Salminen S, Calder PC, Sanders ME. Expert consensus document. The International Scientific Association for Probiotics and Prebiotics consensus statement on the scope and appropriate use of the term probiotic. Nat Rev Gastroenterol Hepatol. 2014;11:506-514.
2. Hotel ACP, Cordoba A. Health and nutritional properties of probiotics in food including powder milk with live lactic acid bacteria. Prev. 2001;5:1-10.
3. Filidou E, Kandilogiannakis L, Shrewsbury A, Kolios G, Kotzampassi K. Probiotics: Shaping the gut immunological responses. World J Gastroenterol 2024; 30(15): 2096-2108