Bài viết bởi Bác sĩ Hồ Thị Xuân Nga - Trung tâm Tim mạch - Bệnh viện Đa khoa Quốc tế Vinmec Central Park
Bệnh động mạch vành là bệnh tim phổ biến nhất gặp phải ở bệnh nhân phẫu thuật. Ở các nước phương Tây, gần 20% bệnh nhân được phẫu thuật bị các bệnh động mạch vành ở mức độ khác nhau. Tỷ lệ này có xu hướng gia tăng cùng với sự tồi tệ của các bệnh tim mạch và sự già hóa của dân số. Trong nghiên cứu đoàn hệ này, bệnh nhân phẫu thuật mạch máu chiếm một vị trí đặc biệt. Hơn 60% trong số họ có dấu hiệu của bệnh mạch vành và tỷ lệ nhồi máu sau phẫu thuật nằm trong khoảng 4,7 đến 8,5% . Tuy nhiên, loại này có nguy cơ thiếu máu cục bộ rất cao chiếm đến 10% trong tổng số bệnh nhân phẫu thuật.
1. Bệnh động mạch vành
Loại, mức độ nghiêm trọng và tỷ lệ mắc bệnh động mạch vành thay đổi tùy theo dân số. Ví dụ, trong trường hợp phình động mạch chủ bụng, tỷ lệ đau thắt ngực lâm sàng là 20% ở Pháp và 49% ở Thụy Điển, và nhồi máu lần lượt là 16% và 50% . Tỷ lệ mắc bệnh động mạch vành bằng 0 ở người Eskimo. Ở Nhật Bản, chỉ bằng 1/10 so với châu Âu và Hoa Kỳ, nhưng tỷ lệ biến chứng tim sau phẫu thuật ở những quần thể này không khác nhau từ lục địa này sang lục địa khác. Đáp ứng với điều trị cũng không đồng nhất: ở Bắc Mỹ, chẳng hạn, dân số da đen đáp ứng kém hơn với thuốc chẹn beta so với dân số da trắng.
Nói chung, mối quan hệ giữa các sự kiện phẫu thuật và nhồi máu sau phẫu thuật là đa yếu tố. Nhiều yếu tố được tính đến như:
- Loại dân số (địa lý, dân tộc, nam hay nữ);
- Biến đổi di truyền trong đáp ứng với thuốc;
- Tầm quan trọng của kích thích giao cảm và hội chứng viêm;
- Bệnh lý liên quan (tiểu đường, đa mạch, suy thận);
- Loại phẫu thuật và mức độ rối loạn huyết động;
- Loại chấn thương do thiếu máu cục bộ (mất cân bằng giữa nhu cầu và lượng O2 hoặc vỡ mảng bám không ổn định);
- Chất lượng chăm sóc y tế.
2. Hẹp động mạch vành
2.1 Sinh lý bệnh học hẹp mạch vành:
Hẹp động mạch vành là kết quả của một mảng xơ vữa đôi khi đi kèm với sự co thắt của cơ tim. Xơ vữa động mạch là một phản ứng viêm mãn tính gây ra bởi sự rối loạn chức năng nội mô, được đặc trưng bởi mức độ protein phản ứng C quá mức và các kích thích sinh hóa như cholesterol LDL (lipoprotein trọng lượng thấp) gặp nhiều ở bệnh nhân hút thuốc lá hoặc bệnh tiểu đường. Rối loạn chức năng nội mô có liên quan đến khuynh hướng di truyền và tình trạng căng thẳng (tăng huyết áp). Nó dẫn đến sự xâm nhập của đại thực bào chứa cholesterol trọng lượng phân tử thấp (tế bào bọt) vào tế bào cơ trơn mạch máu tạo nên một nang sợi ít nhiều có khả năng chống vỡ khi va đập, cô lập tổn thương từ dòng máu. Các rối loạn chức năng nội mạc này sẽ đi kèm với việc mất chức năng chống đông máu và giãn mạch, tăng kích hoạt sự kết dính tiểu cầu cục bộ.
2.2 Hẹp ổn định và mảng bám không ổn định:
Hẹp động mạch vành có liên quan đến sự tồn tại của hai loại mảng bám:
Mảng xơ vữa ổn định:
Đặc trưng bởi một phần trung tâm lipid nhỏ, được phủ một lớp cơ xơ dày, đôi khi bị vôi hóa. Nó thường gây ra hẹp nặng (> 75 %), có thể thấy rõ trên chụp động mạch, phát triển dần dần và hạn chế lưu lượng máu trên toàn khu vực, dẫn đến nhồi máu không Q với ST chênh lên.
- Chịu trách nhiệm cho 50-60% nhồi máu sau phẫu thuật (tỷ lệ mắc cao nhất: sau ngày thứ 3 hậu phẫu);
- Điều trị dự phòng: DO2, ↓ MVO2, β-blockers.
Mảng xơ vữa không ổn định:
Tăng trưởng không liên tục và không đều, bao gồm một phần trung tâm lớn của chất béo có hàm lượng cholesterol cao (LDL), trong đó các đại thực bào và các yếu tố mô trộn lẫn; khối này được bao bọc yếu bởi một lớp sợi mỏng (50-65 mcm) có dấu hiệu xói mòn và sẹo. Khi chụp động mạch, mảng bám này chỉ biểu hiện bằng hẹp trung bình (≤ 50%) và không giới hạn dòng chảy phía hạ nguồn, bởi vì nó có xu hướng phình ra ngoài và không đi vào trong động mạch [21]. Nguy cơ của nó phụ thuộc vào hoạt động viêm và tính nhạy cảm của nó đối với vỡ, nhưng không phụ thuộc vào mức độ hẹp mà nó gây ra.
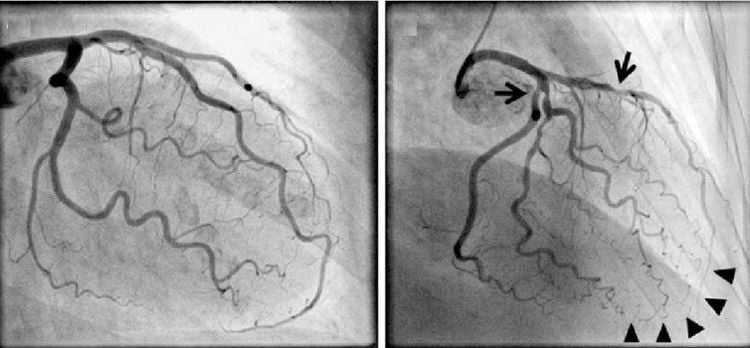
- Ít gây hẹp nặng (<60%), không ảnh hưởng đến DO2; đau thắt ngực hiếm gặp;
- Hẹp không đáng kể khi chụp động mạch, thường là test gắng sức âm tính;
- Mất ổn định, vỡ và huyết khối của động mạch (thiếu máu cục bộ);
- Dẫn đến nhồi máu với sóng Q và ST chênh lên (STEMI);
- Chịu trách nhiệm cho 40-50% nhồi máu sau phẫu thuật (<36 giờ sau phẫu thuật);
- Điều trị dự phòng: thuốc chống tiểu cầu, statin.
3. Những yếu tố nguy cơ gây nên thiếu máu cục bộ
- Mức độ tắc nghẽn dòng chảy ở bệnh nhân có hẹp nặng, ổn định;
- Mức độ không ổn định của một mảng xơ vữa không ổn định;
- Mức độ và vị trí của vùng cơ tim thiếu máu cục bộ;
- Yếu tố thể dịch (kết tập tiểu cầu, hội chứng viêm, căng thẳng).
4. Thiếu máu cơ tim
Thiếu máu cục bộ là tổn thương mô do mất cân bằng giữa cung (DO2) và nhu cầu (VO2) đối với oxy, nguyên nhân có thể do:
- Sự sụt giảm nguồn cung oxy DO2: co thắt mạch máu, hẹp khít, tắc nghẽn do huyết khối, hạ huyết áp, thiếu máu, thiếu oxy.
- Sự tăng nhu cầu oxy VO2 được liên quan đến: nhịp tim nhanh, tăng sức căng của thành và sức co bóp, căng thẳng, đau đớn.
Thiếu máu cục bộ gây ra các sự kiện sau trong <5 phút, theo thứ tự thời gian:
- Rối loạn chức năng tâm trương,
- Giảm vận động vùng,
- Rối loạn chức năng tâm thu,
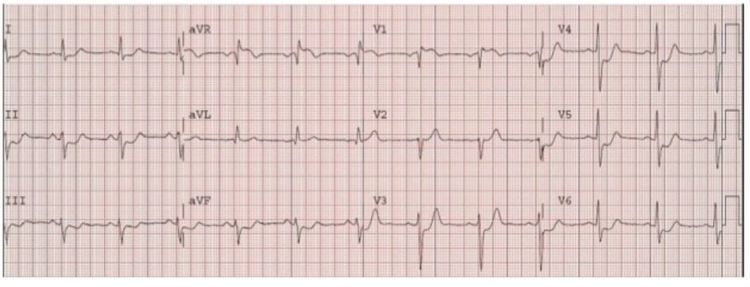
- Thay đổi ST (ECG),
- Đau ngực (do phóng thích adenosine).

Khi dòng chảy mạch máu bị gián đoạn> 20 phút sẽ gây ra hoại tử (trong trường hợp không có tuần hoàn phụ). Ảnh hưởng lên huyết động phụ thuộc vào khối tâm thất bị tổn thương: 25% gây ra suy thất và> 35% gây ra sốc tim.
Hội chứng mạch vành cấp tính được xác định bởi vị trí của đoạn ST: chênh lên (nhồi máu STEMI) hoặc chênh xuống (nhồi máu không STEMI). Nhồi máu được xác định bởi sự gia tăng của men tim.
Nhồi máu là hoại tử mô xảy ra sau 20 phút tắc mạch vành hoàn toàn. Với sự có mặt của tuần hoàn phụ, thời gian này được kéo dài đến 4 - 6 giờ. Hiện tượng sẽ nặng hơn nếu mVO2 cao hoặc huyết áp hệ thống thấp.
Những thay đổi trong giảm vận động vùng phụ thuộc vào độ dày của vùng bị ảnh hưởng: 20% gây ra chứng giảm vận động và ≥ 40% gây ra vô động. Chỉ số EF giảm nếu ≥ 15% khối lượng thất (T) bị nhồi máu. Trong giai đoạn cấp tính, khu vực giáp ranh vùng nhồi máu sẽ tăng rộng kích thước của giảm hoặc vô động nhưng có khả năng phục hồi sau khi tái tưới máu.
Có 2 loại nhồi máu tùy thuộc vào việc có hay không có sóng Q trên ECG và theo nguyên nhân của một mảng bám ổn định (mất cân bằng DO2 / mVO2) hoặc một mảng bám không ổn định (huyết khối).
- Trên lâm sàng bệnh lý tim mạch: 2/3 nhồi máu là do vỡ mảng bám không ổn định, (ST chênh lên > 1 mm, nhồi máu STEMI, sự hiện diện của sóng Q);
- Sau phẫu thuật: 50-60% là do mất cân bằng DO2 / mVO2 (ST chênh xuống >1 mm, nhồi máu không STEMI).
Mời quý vị xem thêm loại bài về “Gây mê hồi sức trong bệnh cơ tim thiếu máu và tái tưới máu mạch vành” của Bác sĩ Hồ Thị Xuân Nga:
- Gây mê hồi sức trong bệnh cơ tim thiếu máu và tái tưới máu mạch vành - Phần 1
- Gây mê hồi sức trong bệnh cơ tim thiếu máu và tái tưới máu mạch vành - Phần 2
- Gây mê hồi sức trong bệnh cơ tim thiếu máu và tái tưới máu mạch vành - Phần 3
TÀI LIỆU THAM KHẢO
- FLEISHER LA, BECKMAN JA, BROWN KA, et al. ACC/AHA 2007 Guidelines on perioperative cardiovascular evaluation and care for non-cardiac surgery: Executive summary. J Am Coll Cardiol 2007; 50:1707-32
- GROSSMAN W, ed. Cardiac catheterization and angiography. 3rd edition. Philadelphia, Lea and Febiger, 1986, 378
- KAPLAN Joel.A, Cardiac Anesthesia for cardiac and non-cardiac surgery, 7th edition. Elservier, 2017, 1453-236
- KERTAI MD, BOUTIOUKOS M, BOERSMA M, et. Aortic stenosis: An underestimated risk factor for perioperative complications in patients undergoing noncardiac surgery. Am J Med 2004; 116:8-13
- KWAK J, ANDRAWES M, GARVIN S, et al. 3D transesophageal echocardiography: a review of recent literature 2007-2009. Curr Opin Anesthesiol 2010; 23:80-8
- MILLER FA. Aortic stenosis: Most cases no longer require invasive hemodynamic study. J Am Coll Cardiol 1989; 13:551-8
- STS – Society of Thoracic Surgeons National Cardiac Surgery Database, 2005. http://www.sts.org/documents/pdf/STS-ExecutiveSummary.pdf
- TIMMIS SB, KIRSH MM, MONTGOMERY DG, STARLING MR. Evaluation of left ventricular ejection fraction as a measure of pump performance in patients with chronic mitral regurgitation. Cathet Cardiovasc Intervent 2000; 49:290-7
- TORNOS MP, OLONA M, PERMAYER-MIRALDA G, et al. Heart failure after aortic valve replacement for aortic regurgitation: prospective 20-year study. Am Heart J 1998; 136:681-7
Để đặt lịch khám tại viện, Quý khách vui lòng bấm số HOTLINE hoặc đặt lịch trực tiếp TẠI ĐÂY. Tải và đặt lịch khám tự động trên ứng dụng MyVinmec để quản lý, theo dõi lịch và đặt hẹn mọi lúc mọi nơi ngay trên ứng dụng.