Bài viết bởi Thạc sĩ, Bác sĩ Mai Viễn Phương - Khoa Khám bệnh & Nội khoa - Bệnh viện Đa khoa Quốc tế Vinmec Central Park
Ung thư biểu mô tuyến tụy (PDAC) mang lại tỷ lệ mắc bệnh và tử vong đáng kể và vẫn là một trong những khối u ác tính khó điều trị nhất. Các yếu tố của từng bệnh nhân và khối u cần được tính đến để đưa ra phương pháp tối ưu, được cá nhân hóa. Trong bài tổng quan này, chúng tôi nêu bật các dấu ấn sinh học đã được thiết lập và mới có tiềm năng được sử dụng làm dấu ấn sinh học tiên lượng trong ung thư biểu mô tuyến tụy và một số có thể được sử dụng để hướng dẫn các quyết định điều trị.
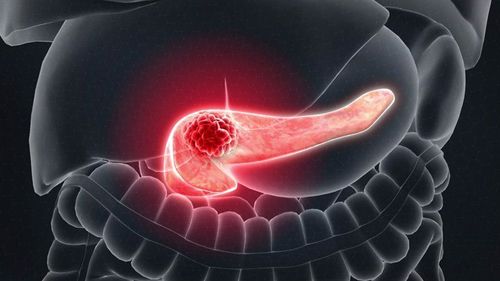
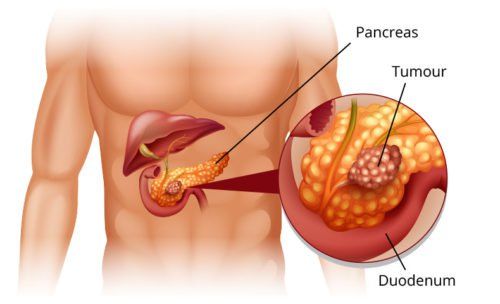
1. Tổng quan về ung thư biểu mô tuyến tụy
Bất chấp những tiến bộ lớn trong phương pháp điều trị nhiều khối u đặc, tỷ lệ sống sót trong ung thư biểu mô tuyến tụy vẫn không được cải thiện. Chẩn đoán chậm trễ, sinh học tích cực và kháng hóa chất rõ rệt đều góp phần vào xu hướng đáng thất vọng này. Các dấu ấn sinh học tiên lượng thông báo về khả năng xảy ra ung thư (bệnh tái phát, tiến triển hoặc tử vong) độc lập với loại điều trị.
Một dấu ấn sinh học có tính chất dự đoán nếu có sự khác biệt về hiệu quả điều trị ở bệnh nhân dương tính với dấu ấn sinh học so với bệnh nhân âm tính với dấu ấn sinh học. Các dấu hiệu tiên lượng chung, không đặc hiệu cho một chế độ điều trị xác định, có thể hữu ích trong việc phân biệt bệnh nhân nào có nguy cơ cao bị kết cục xấu và do đó cần được quản lý tích cực hơn. Trong khi các bảng biểu hiện gen lớn đã được xác định để sử dụng trong việc tiên lượng các khối u ác tính khác và một số có liên quan đến đáp ứng điều trị, một số dấu hiệu như vậy đã được đặc trưng tốt trong ung thư tuyến tụy và thậm chí ít hơn được sử dụng trong thực hành lâm sàng.
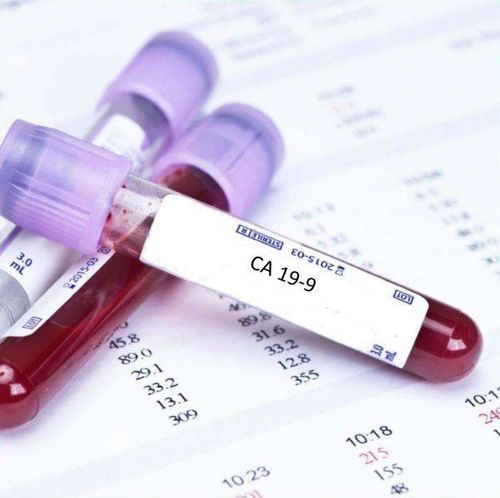
2. Các dấu ấn sinh học dựa trên huyết thanh (xét nghiệm máu)
Có rất ít dấu ấn sinh học được sử dụng rộng rãi trên lâm sàng cho ung thư biểu mô tuyến tụy so với các khối u ác tính khác. Kháng nguyên carbohydrate 19-9 (CA 19-9), hoặc kháng nguyên sialyl Lewis, là dấu ấn sinh học duy nhất được khuyến nghị bởi các hướng dẫn của Mạng lưới Ung thư Toàn diện Quốc gia trong việc đánh giá ung thư biểu mô tuyến tụy . Vai trò của nó trong sinh ung thư có thể liên quan đến mối liên hệ của nó với sự gia tăng sự gắn bó của tế bào ung thư với tế bào nội mô thông qua E-selectin. Ngoài vai trò nổi tiếng của nó trong chẩn đoán ung thư biểu mô tuyến tụy , nồng độ CA trước phẫu thuật cao hơn đã được chứng minh là có tương quan với giai đoạn tiến triển, ít khả năng nối lại, và giảm tỷ lệ sống sót. Tuy nhiên, độ nhạy của nó bị hạn chế do 10% dân số là người không tiết CA 19-9 và tính đặc hiệu của nó bị hạn chế do được biểu mô mật bình thường tiết ra.
Các chỉ số xét nghiệm trước phẫu thuật thường được sử dụng khác bao gồm kháng nguyên carcinoembryonic (CEA), glycoprotein kết dính gian bào thường có ở mức độ rất thấp trong máu, lactate dehydrogenase (LDH), một loại enzyme liên quan đến chuyển hóa đường và protein phản ứng C (CRP), một chất phản ứng giai đoạn cấp tính. So với mức bình thường, LDH, CEA, và CRP tăng đều được chứng minh là các yếu tố tiên lượng sống còn bất lợi độc lập. Tuy nhiên, tương tự như CA 19-9, các dấu hiệu phòng thí nghiệm này bị hạn chế về tính đặc hiệu.
3. Dấu ấn sinh học dựa trên máu hoặc huyết thanh đang phát triển
Giá trị của các chất đánh dấu dựa trên huyết thanh là cách tiếp cận ít xâm lấn của chúng và khả năng thu thập nhiều mẫu cho các phân tích khác nhau. Các chất chỉ điểm dựa trên huyết thanh đáng chú ý nhất hiện đang được nghiên cứu bao gồm các tế bào khối u đang lưu hành, DNA khối u lưu hành và microRNA.
Sự di căn thường được coi là một trong những bước mới nhất trong sự tiến triển của ung thư ; tuy nhiên, sự hiện diện của các tế bào khối u lưu hành (CDC ) trong giai đoạn đầu cũng như trong các tổn thương trước xâm lấn đã thách thức điều này. Tế bào khối u lưu hành là các tế bào ung thư bị bong ra khỏi khối u nguyên phát hoặc di căn và có thể di chuyển theo dòng máu, có khả năng dẫn đến di căn mới.
4. Dấu ấn sinh học dựa trên mô học
Sinh thiết u tụy chất lượng cao
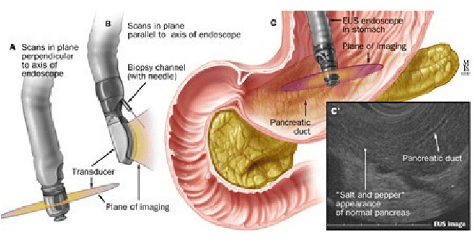
Gần đây đã có những tiến bộ rõ rệt trong khả năng thu được sinh thiết lõi nguyên vẹn về mặt mô học từ ung thư tuyến tụy và sự thay đổi này có thể sẽ cho phép sử dụng nhiều hơn các dấu ấn sinh học dựa trên mô. Mặc dù có rất ít nghiên cứu đánh giá các kỹ thuật sinh thiết và thiết kế kim khác nhau song song với nhau, nhưng rõ ràng là sinh thiết kim siêu nhỏ “lõi” thế hệ mới hơn (FNB) sẽ cung cấp các mẫu vật có chất lượng và số lượng tốt hơn nhiều so với sinh thiết kim nhỏ thế hệ đầu tiên ( FNA).
Một số nghiên cứu đã chứng minh rằng độ chính xác chẩn đoán tổng thể của FNA và FNB là tương đương nhau (tương ứng là 92,5- 94,8% so với 90-98,3%). Trong một số nghiên cứu, FNB yêu cầu số lần đi kim thấp hơn đáng kể và có liên quan đến độ chính xác cao hơn khi xét nghiệm tế bào học tại chỗ. Tuy nhiên, nhiều nghiên cứu gần đây đã tìm thấy độ chính xác chẩn đoán tổng thể tương tự nhau và độ chính xác chẩn đoán theo đường dẫn.
5. Các dấu ấn đánh giá tiên lượng
Các chất đánh dấu dựa trên mô mang lại lợi ích là cụ thể hơn đối với mô khối u, nhưng với chi phí đòi hỏi các kỹ thuật thu thập xâm lấn hơn. Phân tích hóa mô miễn dịch (IHC) là một quy trình được sử dụng rộng rãi được sử dụng để hình dung các chỉ thị phân tử cụ thể và xác định sự phân bố của chúng trong các mẫu mô lâm sàng.
Mặc dù những dấu ấn này có thể hữu ích ở những bệnh nhân trải qua phẫu thuật cắt bỏ, vẫn cần điều tra để xác định xem liệu có giá trị tiên lượng đối với những dấu ấn sinh học này trong mẫu bàn chải hoặc sinh thiết trước phẫu thuật hay không.
Yếu tố SPARC
Protein tiết ra có tính axit và giàu cysteine (SPARC) là một glycoprotein tế bào gốc trải qua giai đoạn im lặng biểu sinh trong ung thư biểu mô tuyến tụy, nhưng thường biểu hiện mạnh mẽ ở mặt phân cách giữa khối u và mô đệm bởi nguyên bào sợi mô đệm. Dữ liệu hỗ trợ cho thấy sự tương tác này rất quan trọng đối với sự tiến triển của khối u, sự di căn và độ bền hóa học.
Biểu hiện mô đệm SPARC được quan sát thấy trong tất cả các giai đoạn bệnh cho thấy biểu hiện sớm là rất quan trọng đối với sự tiến triển của khối u. Biểu hiện SPARC mô đệm mạnh ở những bệnh nhân ung thư biệt hóa từ khá đến trung bình đã trải qua phẫu thuật cắt bỏ có liên quan đến việc giảm tỷ lệ sống thêm so với những bệnh nhân không có biểu hiện SPARC. Hơn nữa, những bệnh nhân có biểu hiện SPARC mô đệm lan tỏa ra ngoài vùng quanh bụng có tiên lượng xấu hơn đáng kể.
Yếu tố Smad4
Smad4 là một gen ức chế khối u liên quan đến trung gian chuyển đổi yếu tố tăng trưởng beta (TGF-B). Được chứng minh bằng tên thay thế của nó, DPC4 (bị xóa trong ung thư biểu mô tuyến tụy, vị trí 4), mất hoặc bất hoạt Smad4 được thấy ở ∼50% ung thư biểu mô tuyến tụy và dẫn đến tăng sinh tế bào bằng cách điều chỉnh sự tiến triển từ G1-S trong chu kỳ tế bào. Mất biểu hiện Smad4 thường được chứng minh là có liên quan đến giảm khả năng sống sót trong ung thư biểu mô tuyến tụy .
Thật thú vị, một nghiên cứu đã chứng minh một cách trái ngược rằng biểu hiện Smad4 thấp có liên quan đến khả năng sống sót chung được cải thiện và quan trọng là, việc cắt bỏ tuyến tụy chỉ có lợi (thông qua thời gian sống lâu hơn) những khối u đã mất biểu hiện Smad4.
Yếu tố KRAS
KRAS (V-Ki-ras2 Kirsten chuột đồng gen sinh ung thư sarcoma của chuột) là một GTPase kích hoạt các protein cần thiết để truyền các yếu tố tăng trưởng và các thụ thể tín hiệu tế bào khác. Nhìn chung, đột biến KRAS có tương quan với việc giảm tỷ lệ sống sót. Các kiểu phụ đột biến khác nhau cho thấy thời gian sống sót khác nhau, trong đó loại GGT hoang dã (glycine) được chuyển đổi thành GAT (aspartate) là loại phổ biến nhất và là loại duy nhất được tiên lượng về khả năng sống sót kém.
Ngoài ra, phân tích đột biến được thực hiện cho các đột biến KRAS này có thể được thực hiện bằng phản ứng chuỗi polymerase định lượng (PCR), rẻ hơn và nhanh hơn các phương pháp giải trình tự khác và sử dụng ít dữ liệu DNA hơn, giúp dễ dàng thực hiện nhiều phân tích phân tử trên cùng một mẫu.
Smad4, hENT1 và SPARC có một lợi ích khác là dấu ấn sinh học, trong đó chúng đã được chứng minh là được đánh giá hiệu quả trên các mẫu sinh thiết trước phẫu thuật. Vì PCR định lượng VEGF và KRAS cũng đã được chứng minh là chính xác, có thể có vai trò của các dấu ấn sinh học này trong quá trình đánh giá trước phẫu thuật với các mẫu nhỏ hơn liên quan đến sinh thiết.
6. Dấu ấn sinh học dự đoán điều trị
Có nhiều phương thức hình ảnh khác nhau liên quan đến chẩn đoán và phân giai đoạn ung thư biểu mô tuyến tụy bao gồm chụp cắt lớp vi tính (CT), chụp cộng hưởng từ (MRI), siêu âm nội soi (EUS) và nội soi mật tụy ngược dòng (ERCP). Vai trò của các phương thức này đã thay đổi theo thời gian, nhưng tầm quan trọng tương đối của EUS đã tăng lên đáng kể với sự ra đời của phương pháp chọc hút kim tinh có hướng dẫn EUS (EUS-FNA) hơn 20 năm trước. Mặc dù bị hạn chế bởi tính xâm lấn tương đối và sự thay đổi của người vận hành, nó đã được chứng minh là có độ nhạy tuyệt vời (91-100%) và độ đặc hiệu (94-100%) để chẩn đoán ung thư biểu mô tuyến tụy .
7. Vai trò chất ức chế VEGF, Vatalinib và nab-paclitaxel
Ngoài ra, từ nhiều thuật toán điều trị ung thư khác, các tác giả biết rằng việc hiểu được những thay đổi trong sinh học khối u theo phác đồ điều trị đầu tiên là rất quan trọng. Các thử nghiệm giai đoạn II gần đây về chất ức chế VEGF, Vatalinib và nab-paclitaxel như là liệu pháp điều trị dòng thứ hai riêng lẻ trong ung thư biểu mô tuyến tụy nâng cao đã chứng minh một kết quả sống còn thuận lợi ở một số bệnh nhân; tuy nhiên, dấu ấn sinh học dựa trên huyết thanh không tương quan với đáp ứng và giá trị dự đoán của dấu ấn sinh học dựa trên mô (SPARC) không kết luận được do kích thước mẫu nhỏ. Với sinh thiết chất lượng cao, chúng ta có thể mong đợi rằng hầu hết các thử nghiệm, và ngày càng tiêu chuẩn thực hành, sẽ nhấn mạnh sự cần thiết của sinh thiết sau điều trị.
PHẦN KẾT LUẬN
Các dấu ấn sinh học mô hứa hẹn nhất bao gồm hENT1, SPARC, Smad4 và VEGF vì chúng có thể có giá trị trong giai đoạn trước phẫu thuật và cũng có thể có giá trị tiên đoán trong việc hướng dẫn điều trị ung thư tuyến tụy cá thể. Các dấu ấn dựa trên huyết thanh mới cũng có giá trị do cách tiếp cận xâm lấn tối thiểu và là nền tảng để phân tích di truyền. Vì cả hai phương pháp nội soi để lấy các mẫu sinh thiết chất lượng cao và sự hiểu biết về phân tử của bệnh ung thư tuyến tụy tiến bộ, có khả năng những phương pháp này và nhiều dấu ấn sinh học khác sẽ được đưa vào thực hành lâm sàng thường quy.
Bệnh viện Vinmec với cơ sở vật chất và trang thiết bị hiện đại cùng đội ngũ chuyên gia giàu kinh nghiệm, luôn tận tâm tận lực trong khám chữa bệnh, khách hàng có thể yên tâm với dịch vụ nội soi dạ dày, thực quản tại Bệnh viện Đa khoa Quốc tế Vinmec.
Tài liệu tham khảo
- Yadav D, Lowenfels AB. The epidemiology of pancreatitis and pancreatic cancer. Gastroenterology. 2013;144(6):1252- 1261.
- Swords DS, Firpo MA, Scaife CL, Mulvihill SJ. Biomarkers in pancreatic adenocarcinoma: current perspectives. Onco Targets Ther. 2016;9:7459-7467.
- Ferrone CR, Finkelstein DM, Thayer SP, Muzikansky A, Fernandez-delCastillo C, Warshaw AL. Perioperative CA19-9 levels can predict stage and survival in patients with resectable pancreatic adenocarcinoma. J Clin Oncol. 2006;24(18):2897-2902.
Để đặt lịch khám tại viện, Quý khách vui lòng bấm số HOTLINE hoặc đặt lịch trực tiếp TẠI ĐÂY. Tải và đặt lịch khám tự động trên ứng dụng MyVinmec để quản lý, theo dõi lịch và đặt hẹn mọi lúc mọi nơi ngay trên ứng dụng.