Bài viết được viết bởi Tiến sĩ, Bác sĩ Bùi Xuân Trường - Khoa Nội tổng hợp - Bệnh viện Đa khoa Quốc tế Vinmec Times City.
So với một số virus viêm gan khác, virus viêm gan C (HCV: hepatitis C virus) được phát hiện khá muộn, vào năm 1989, hiện nay có khoảng 150 – 170 triệu người trên thế giới nhiễm virus viêm gan C mạn tính, hàng năm có khoảng 500.000 bệnh nhân tử vong do các bệnh liên quan đến viêm gan C. Cùng với virus viêm gan B và rượu, virus viêm gan C là một trong ba nguyên nhân hàng đầu gây nên viêm gan mạn, xơ gan và ung thư gan.

1. Tại sao chúng ta cần chú ý đến bệnh lý viêm gan C
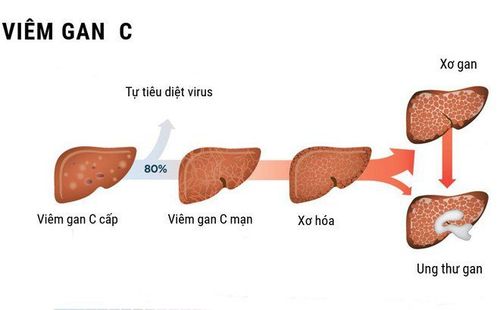
Khi bị nhiễm HCV cấp tính, tỷ lệ chuyển thành mạn tính khá cao, khoảng 55-85% và nếu không được điều trị, kiểm soát thì sau khoảng 20 năm sẽ có 15-30% số bệnh nhân nhiễm HCV mạn tính sẽ phát triển thành xơ gan. Trên nền xơ gan do HCV, hàng năm có khoảng 2-4% sẽ phát triển thành ung thư gan. Ngoài ra nhiễm HCV có thể gây nên một số bệnh lý ngoài gan, các bệnh lý này chủ yếu là hậu quả của sự đáp ứng miễn dịch của cơ thể đối với HCV.
Trên khía cạnh vaccince phòng bệnh còn gặp nhiều khó khăn, do HCV có tính đa hình thái kiểu gen rất cao (HCV có 07 kiểu gene và mỗi một loại kiểu gene lại có khá nhiều phân nhóm dưới kiểu gene), bên cạnh đó HCV không có nhóm quyết định kháng nguyên chung giống như virus viêm gan B (HBV: hepatitis B virus), do vậy hiện nay Y học chưa thể tạo ra được một loại vaccine để tiêm phòng cho tất cả các chủng HCV trên toàn thế giới.
Mặc dù còn gặp nhiều khó khăn trong việc tạo vaccine phòng bệnh và có tới 55-85% số bệnh nhân nhiễm HCV cấp tính sẽ chuyển thành nhiễm HCV mạn tính. Tuy vậy so với viêm gan B, chúng ta hoàn toàn có thể làm sạch được HCV ra khỏi cơ thể, và với sự tiến bộ gần đây trong việc tạo ra các thuốc mới trong điều trị viêm gan C, một số quốc gia đang phấn đấu đưa ra lộ trình tiến tới xóa bỏ được bệnh viêm gan C.
2. Kiến thức căn bản về cấu trúc của virus viêm gan C
Virus viêm gan C (HCV: hepatitis C virus) thuộc nhóm Hepacivirus họ Flaviviridea (trong họ Flaviviridea còn hai nhóm khác là Flavivirus và Pestivirus) các virus thuộc họ Flavividea có một số đặc điểm cấu trúc cơ bản giống nhau, tuy nhiên các virus khác nhau có vị trí gây bệnh và đặc điểm bệnh lý khác nhau.

- Virus viêm gan C (HCV) có lớp vỏ ngoài cùng là loại màng lipid kép (lipid bilayer) – xuyên cắm vào lớp màng lipid kép này là các phân tử protein (E) trông giống những gai hình mỏ neo lồi ra phía bên ngoài virus
- Phía bên trong lớp vỏ lipid kép là lớp màng lõi (nucleocapsid layer – Core protein)
- Bên trong lớp màng lõi là sợi đơn RNA (chứa đựng thông tin di truyền của virus)
Phân tử RNA của HCV (HCV-RNA) có chiều dài khoảng 9600 nt hay 9,6 kb (nt là từ viết tắt của nucleotide và kb là từ viết tắt của kilobase) và mã hóa cho khoảng 3300 amino acid (aa) – tuy nhiên có thể có sự thay đổi đôi chút, sự thay đổi này tùy thuộc vào kiểu gen của HCV. Giới hạn của phân tử HCV-RNA là hai đầu tận 5’URT và 3’URT. Đầu tận 5’URT có chiều dài khoảng 341 nt và đầu tân 3’URT có chiều dài khoảng 225 nt, hai đầu tận 5’URT và 3’URT không tham gia trực tiếp làm nhiệm vụ mã hóa các phân tử amino acid, tuy nhiêu đầu tận 5’URT có vai trò quan trọng trong tiến trình khởi động dịch mã thông tin của HCV-RNA và 3’URT tham gia tạo hiệu ứng tín hiệu cho quá trình nhân lên của HCV-RNA.

Phân tử HCV-RNA chỉ bao gồm một khung chứa đựng thông tin di chuyền – giải mã và dịch mã thông tin di truyền liên tiếp nhau (ORF: open reading frame), HCV-RNA mã hóa cho khoảng 11 phân tử protein của HCV và được chia làm 02 phần chính, phần chứa đựng thông tin di truyền mã hóa cho các phân tử protein tạo cấu trúc HCV (structural proteins) bao gồm: C (core protein), E1 (protein E1) và E2 (protein E2), và phần chứa đựng thông tin di truyền mã hóa cho các phân tử protein không tạo cấu trúc (non-structural proteins) HCV bao gồm: NS2 (protein NS2), NS3 (protein NS3), NS4A (protein NS4A), NS4B (protein NS4B), NS5A (protein NS5A) và NS5B (protein NS5B). Protein P7 không tham gia tạo cấu trúc HCV – tuy hiện nay chức năng của protein P7 còn nhiều điểm chưa được biết đến, một số nghiên cứu cho thấy protein P7 có vai trò như một kênh calci.
3. Sơ lược căn bản về quá trình nhân lên của virus viêm gan C
Cho đến nay Y học đã có nhiều bước tiến, đạt được nhiều thành công trong nghiên cứu quá trình nhân lên của HCV trong cơ thể con người, tuy vậy vẫn còn nhiều vấn đề và cơ chế chúng ta chưa nhận biết và phân tích được. Để quá trình nhân lên được hoàn thành, HCV bắt buột phải có sự tương tác và hỗ trợ từ một số hoạt động bao gồm cả ở trên bề mặt và trong bào tương của tế bào gan, để hoàn thiện thiện được đủ cấu trúc thì HCV phải sử dụng một số sản phẩm bên trong tế bào gan, tuy có nhiều quá trình là nội bào tương nhưng hoàn toàn ở ngoài nhân tế bào và HCV-RNA không có sự tích hợp và tương tác với phân tử DNA của tế bào gan như virus viêm gan B.

Quá trình nhân lên của HCV gồm các bước sau:
(1).HCV tiếp cận, gắn lên bề mặt màng tế bào gan và tiếp đó là quá trình hòa màng.
(4).Phân tử HCV-RNA di chuyển đến hệ thống lưới nội bào tương của tế bào gan – tại đây diễn ra quá trình dịch mã tổng hợp nên các phân tử protein của HCV.
(2).Tiểu thể HCV với lớp vỏ nucleocapsid chui vào trong bào tương tế bào gan.
(5).Tiếp đến là quá trình sao chép tổng hợp nên các phân tử HCV-RNA mới.
(3).Phân tử HCV-RNA thoát ra khỏi lớp vỏ nucleocapsid.
(6).Cuối cùng là giai đoạn đóng gói, tạo nên các tiểu thể HCV hoàn chỉnh và sau đó thoát ra khỏi tế bào gan.
4. Các mốc thời gian và thành tựu đạt được trong nghiên cứu phát triển thuốc điều trị viêm gan C
1991: Intron A (Alpha Interferon của công ty Shering ) được cơ quan quản lý thuốc và thực phẩm Hoa kỳ (FDA: Food and Drug Administration) thông qua điều trị viêm gan C trong thực hành lâm sàng.
1996: Roferon A (Alpha Interferon của công ty Roche) được FDA thông qua.
1997: Consnsus Interferon được FDA thông qua.
Tuy nhiên sự áp dụng đơn thuần các thuốc alpha-interferon đạt được hiệu quả điều trị (sau 06 tháng) tương đối thấp, tỷ lệ đáp ứng đối với HCV kiểu gen 1 chỉ khoảng 9-10% và đối với kiểu gen 2 và 3 chỉ khoảng 20-30%. Đồng thời alpha-interferon có khá nhiều tác dụng phụ, nhiều bệnh nhân đã phải bỏ không tham gia điều trị được hết liệu trình.
Bản chất của Interferon là protein có chức năng miễn dịch, thuộc nhóm Cytokines, đây chính là một trong các nhóm chất do bản thân cơ thể chúng ta sản sinh ra, các chất này tham gia vào quá trình điều hòa miễn dịch và đáp ứng miễn dịch nhằm loại bỏ các tác nhân gây bệnh, trong đó có cả nhóm tác nhân do virus. Cơ thể chúng ta có thể tạo ra nhiều loại Interferon khác nhau (type I – type II and type III)– trong đó loại Interferon áp dụng trong điều trị viêm gan C chỉ là Alpha-Interferon thuộc type I và bản thân Alpha-Interferon có nhiều nhóm nhỏ khác nhau mà Alpha-Interferon-2a hay 2b chỉ là một trong số đó (có khoảng 13 gene mã hóa alpha-interferon).
1998: FDA thông qua việc kết hợp Ribavirin với Interferon trong điều trị viêm gan C.
Với phác đồ kết hợp hiệu quả điều trị đã được cải thiện đáng kể, tỷ lệ đáp ứng điều trị đối với HCV kiểu gen 1 đạt khoảng 30% và đối với kiểu gen 2, 3 đạt khoảng 60%.
Ribavirin là thuốc ức chế virus phổ rộng, ban đầu được kỳ vọng phát triển để điều trị bệnh nhân nhiễm virus HIV, tuy nhiên sau này các tác giả nhận thấy Ribavirin không có khả năng điều trị bệnh nhân HIV-Aids, mà ngược lại có tác dụng khá tốt đối với virus thuộc họ Flavivirus, trong đó có cả virus viêm gan C.
2001: Peg-Intron (pegylated interferon alpha-2b) của công ty Shering được FDA thông qua.
2002: Pegasys (pegylated interferon alpha-2a) của công ty Roche được FDA thông qua điều trị viêm gan C.
Với sự ra đời của Peg-Interferon (Peg-Intron và Pegasys) đã tạo nên một sự chuyển biến đáng kể trong hiệu quả điều trị viêm gan C. Trước đây với các loại Interferong truyền thống, người bệnh cần phải tiêm thuốc 03 lần/tuần, tuy có rất nhiều tác giả đã cố gắng đưa ra các liệu trình khác nhau – nhưng với các loại Interferon truyền thống rất khó tạo được nồng độ Interferong hằng định trong cơ thể người bệnh trong quá trình điều trị.
Với sự ra đời của Peg-Interferon, người bệnh chỉ cần phải tiêm 01 lần/tuần – đồng thời đạt được hiệu quả nồng độ hằng định Interferon trong cơ thể người bệnh trong quá trình điều trị.
Việc kết hợp Peg-Interferon với Ribavirin đã làm thay đổi hiệu quả điều trị viêm gan C một cách có ý nghĩa, tỷ lệ đáp ứng điều trị bền vững đối với HCV kiểu gen 1 đã tăng lên 40-45% và tỷ lệ đáp ứng điều trị đối với HCV kiểu gen 2 và 3 tăng lên khoảng 75-85%, đối với kiểu gen 4, 5 và 6 khoảng 50-75%.
2007: Đây là năm đánh dấu khởi đầu của sự ra đời của các thế hệ thuốc uống mới, đầu tiên là VX-950 (Telaprevir), thuốc viên dạng uống áp dụng cho điều trị HCV kiểu gen 1.
2010: Telaprevir và Boceprevir kết thúc thử nghiệm lâm sàng giai đoạn III và chính thức đề nghị FDA thông qua cho phép áp dụng điều trị rộng rãi trong lâm sàng viêm gan C.
2011: Telaprevir và Boceprevir chính thức được FDA cấp phép.
2013: Simeprevir và Sofosbuvir được cấp phép.
2014: Ledipasvir được cấp phép.
2015: Daclatasvir được cấp phép, đây cũng là năm đánh dấu bước ngoặt sự phát triển các thuốc, các phác đồ đặc hiệu điều trị cho từng kiểu gen của HCV.
2016: Elbasvir và Grazoprevir được cấp phép.
Hiện nay song hành với sự phát triển nghiên cứu và hiểu biết ngày càng chi tiết hơn, đồng bộ hơn về cấu trúc, chức năng và quá trình sinh bệnh của virus viêm gan C, ngày càng có nhiều thuốc uống thế hệ mới được nghiên cứu thành công và được phép áp dụng trong điều trị lâm sàng. Điều này đã cho phép giảm phụ thuộc hoặc không còn phải phụ thuộc vào các thuốc Interferong trong điều trị, tạo điều kiện thuận lợi - dễ áp dụng - giảm thiểu được tác dụng phụ - dễ được được người bệnh chấp nhận và đạt hiệu quả điều trị cao.
Trong năm 2016 và trong tương lai còn nhiều thuốc mới sẽ được phép áp dụng trong lâm sàng – đây là tín hiệu hết sức khả quan cho bệnh nhân và nhiều nước hy vọng sẽ làm sạch được bệnh lý do virus viêm gan C gây ra.
5. Cơ chế tác dụng của các thuốc uống thế hệ mới trong điều trị viêm gan C
Như phần trên đã trình bày, quá trình nhân lên của HCV bao gồn nhiều bước và phân tử HCV-RNA chỉ bao gồm một khung dịch mã (ORF: open reading frame), tuy nhiên từ một khung dịch mã này có thể tạo nên được nhiều loại protein khác nhau cho HCV, bao gồm cả các proetein tạo cấu trúc và protein không tạo cấu trúc của HCV. Các thế hệ thuốc mới hiện nay chủ yếu tác động vào các protein không tạo cấu trúc của HCV, nhưng các protein này có vai trò quan trọng đối với quá trình xâm nhập, nhân lên và hoàn thiện để HCV thành các virus gây bệnh hoàn chỉnh.
Các thuốc uống thế hệ mới trong bài đề cập đến chính là thuốc thuộc nhóm DAAs (Direct-Acting Antivirals: tác dụng kháng virus trực tiếp).
Các thuốc tác động lên protein NS3/NS4A: Boceprevir, Telaprevir, Simeprevir, Grazoprevir, Faldaprevir và Asunaprevir.............
NS3 vừa có vài trò của protease, NTPase/helicase đồng thời tạo phức hợp với NS4A (trong đó NS4A protease là yếu tố kết hợp hỗ trợ NS3 protease). Phân tử protein ban đầu của HCV tạo ra là một poly-protein, từ phân tử này muốn tạo ra được các phân tử protein đơn của HCV thì cần có quá trình cắt phân tử poly-protein. Phức hợp NS3/NS4A protein có chức năng ly giải cắt phân tử poly-protein tạo ra các sản phẩm protein đơn là NS3, NS4A, NS5A và NS5B. Nếu ức chế phức hợp NS3/NS4A protease thành công sẽ làm mất quá trình này và các sản phẩm protein đơn của HCV sẽ không được tạo ra, chính vì vậy sẽ cắt đứt quá trình nhân lên của HCV. Ngoài ra phức hợp NS3/NS4A protease còn có khả năng ức chế một số con đường đáp ứng miễn dịch của cơ thể thông qua các chuỗi tín hiệu của một số Interferon, do vậy ức chế NS3/NS4A protease cũng chính là làm giải phóng các chuỗi tín hiệu này, làm tăng khả năng đáp ứng miễn dịch của cơ thể đối với HCV.
Các thuốc tác động lên protein NS5A: Daclatasvir, Ledipasvir, Obitasvir.............
Khác với phức hợp NS3/NS4A protease, protein NS5A không có vai trò ly giải để cắt phân tử poly-protein ban đầu thành các phân tử protein đơn, nhưng NS5A tham gia vào quá trình nhân lên của HCV-RNA và quá trình đóng gói tạo nên tiểu thể HCV hoàn thiện. Protein NS5A có 03 phân đoạn chức năng chính (domain I, II và III) trong đó domain I và II tham gia vào quá trình nhân lên của phân tử HCV-RNA và domain III tham gia vào quá trình đóng gói và giải phóng tiểu thể HCV ra khỏi tế bào gan. Do vậy ức chế được NS5A vừa có khả năng ức chế sự nhân lên của HCV – vừa có khả năng ức chế sự đóng gói tạo nên tiểu thể HCV hoàn thiện, đồng thời ức chế sự giải phóng các tiểu thể HCV ra khỏi tế bào gan.
Các thuốc tác động lên protein NS5B: Sofosbuvir, Dasabuvir.............
Sự sao chép tổng hợp phân tử HCV-RNA thuộc cơ chế tổng hợp RNA phụ thuộc RNA polymerase, không phải là quá trình RNA phụ thuộc DNA polymerase. Phân tử protein NS5B của HCV giữ vai trò của một RNA polymerase, do vậy có vai trò then chốt đối với quá trình tổng hợp lên tiền phân tử (-) HCV-RNA (negative HCV-RNA strand) và chính từ phân tử này sẽ tổng hợp nên các phân tử (+) HCV-RNA của virus viêm gan C. Chính vì vậy ức chế NS5B sẽ làm cho quá trình nhân lên của HCV-RNA không diễn ra.
6. Sàng lọc và quản lý người bệnh nhiễm HCV
Để đạt được hiệu quả điều trị và làm giảm tỷ lệ bệnh lý viêm gan C, cần làm tốt công tác sàng lọc và quản lý người bệnh nhiễm HCV
Các đối tượng trong diện cần sàng lọc nhiễm HCV:
(1). Nhân viên y tế và những người làm công tác quản lý xã hội có tiếp xúc với rác thải y tế và các đối tượng có nhiễm HCV.
(2). Người nghiện hút có sử dụng tiêm chích, kể cả sử dụng ma túy dạng hít qua đường mũi.
(3). Bệnh nhân chạy thận nhân tạo.
(4). Bệnh nhân có tiền sử truyền máu và có sử dụng các chế phẩm từ máu, đặc biệt ở những người bệnh sử dụng từ thời kỳ khi xét nghiệm sàng lọc HCV với truyền máu chưa có điều kiện triển khai.
(5). Bệnh nhân ghép tạng.
(6). Trẻ em sinh ra có mẹ nhiễm HCV.
(7). Người nhiễm HIV.
(8). Người có rối loạn chức năng gan và không tìm ra nguyên nhân.
(9). Người có quan hệ tình dục không an toàn, tình dục đồng giới.
(10). Người có thói quen xăm trổ hay sử dụng chung các dụng cụ có dính máu và dịch cơ thể.
Khi muốn tư vấn và điều trị viêm gan C
Khi bạn muốn tư vấn sàng lọc và điều trị viêm gan C, bạn nên đến khám và tư vấn tại các phòng khám hay bệnh viện có chuyên khoa về Tiêu hóa – Gan mật – Viêm gan, chuyên khoa bệnh Truyền nhiễm. Hiện nay tại nhiều cơ sở Y tế trên toàn quốc ngoài những xét nghiệm đánh giá bệnh lý gan, cũng đã triển khai các xét nghiệm ở mức độ phân tử của HCV – giúp ích cho quá trình đánh giá hiệu quả điều trị chính xác.
Bạn không nên tự tham khảo và tự điều trị, vì dù hiện Y học đã đạt được nhiều tiến bộ trong điều trị viêm gan C, nhưng vẫn còn nhiều vấn đề trong cơ chế sinh bệnh học chưa lý giải được hết do vậy vẫn còn tồn tại những khó khăn và thách thức mà Y học cần tiếp tục nghiên cứu. Tự điều trị hoặc được tư vấn điều trị không đúng sẽ làm gia tăng đột biến kháng thuốc.
Bên cạnh đó bạn cần biết viêm gan C là bệnh lý do virus gây ra – do vậy hiện nay đối với các thuốc y học cổ truyền, các thuốc này có thể làm bình ổn chức năng gan, nhưng không có bằng chứng có khả năng loại bỏ được nhiễm HCV mạn tính ra khỏi cơ thể.
Để đặt lịch khám tại viện, Quý khách vui lòng bấm số HOTLINE hoặc đặt lịch trực tiếp TẠI ĐÂY. Tải và đặt lịch khám tự động trên ứng dụng MyVinmec để quản lý, theo dõi lịch và đặt hẹn mọi lúc mọi nơi ngay trên ứng dụng.