Bài viết bởi Thạc sĩ, Bác sĩ Nguyễn Văn Phòng và Tạ Văn Thành - Khối Liệu pháp tế bào, Trung tâm Công nghệ cao Vinmec
Mặc dù các phương pháp tiêu diệt tế bào đích cũng như điều chỉnh phản ứng miễn dịch của tế bào T gây độc và tế bào NK là khá tương đồng, nhưng cơ chế mà chúng xác định mục tiêu là khác nhau.
1. Giới thiệu chung
Tế bào T gây độc và tế bào giết tự nhiên (tế bào NK) là các tế bào bạch cầu lympho, chúng có nguồn gốc từ tủy xương được biệt hóa và phân bố ở nhiều mô cơ quan trong cơ thể như máu ngoại vi, gan, lách, hạch bạch huyết... 2 dòng tế bào đều đóng vai trò quan trọng trong việc kiểm soát nhiễm trùng, phát hiện và loại bỏ các tế bào ung thư.
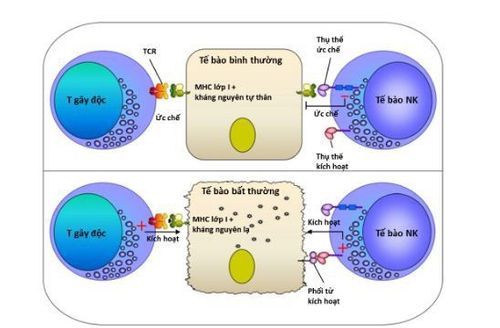
Mặc dù các phương pháp tiêu diệt tế bào đích cũng như điều chỉnh phản ứng miễn dịch của tế bào T gây độc và tế bào NK là khá tương đồng, nhưng cơ chế mà chúng xác định mục tiêu là khác nhau. Tế bào T gây độc nhận biết các tế bào bất thường thông qua liên kết đặc hiệu giữa thụ thể tế bào T (TCR) với kháng nguyên được trình diện trên phân tử MHC lớp I. Khả năng đặc biệt này của tế bào T gây độc được quy định bởi các tế bào trình diện kháng nguyên.
Mặt khác, các tế bào NK có khả năng nhận diện sự vắng mặt/bất thường của phức hệ phù hợp tổ chức chính MHC lớp I trên bề mặt tế bào (Cơ chế trốn tránh tế bào T gây độc của tế bào ung thư, tế bào nhiễm virus). Tế bào NK đóng vai trò quan trọng trong việc phát hiện và tiêu diệt các tế bào bị nhiễm virus và tế bào ung thư mà không cần phải tiếp xúc trước.
2. Sự khác biệt về hình thái và cấu trúc tế bào
Tế bào NK và tế bào T gây độc là các tế bào miễn dịch cùng nguồn gốc, vì vậy chúng có nhiều đặc điểm tương đồng về hình thái và cấu trúc. Một số đặc điểm phân loại của hai dòng tế bào được tổng hợp trong bảng 1.
Bảng 1: Một số đặc điểm phân loại tế bào NK và tế bào T gây độc
| Đặc điểm phân loại | Tế bào NK | Tế bào T gây độc |
| Nguồn gốc | Tế bào đầu dòng lympho, tủy xương | Tế bào đầu dòng lympho, tủy xương |
| Tỷ lệ trong tổng số tế bào lympho trong máu ngoại vi | 5-15% | 20-30% |
| Đường kính tế bào | 6-7μm | 5-6μm |
| Dấu ấn bề mặt tế bào | CD56+, CD3- | CD56-, CD4-, CD3+, CD8+ |
| Biểu hiện MHC lớp I ở tế bào đích | Ức chế hoạt động tế bào | Kích hoạt tế bào, nhận diện tế bào đích |
| Thiếu hụt MHC lớp I ở tế bào đích | Kích hoạt tế bào | Giảm hoặc mất khả năng nhận diện tế bào đích |
| Khả năng ghi nhớ | Không | Có |
| Sản xuất cytokine | IFN-γ, TNF-α, IL-17A, IL-22, Perforin/Granzyme… | IFN-γ, TNF-α, TNF-β, IL-4, IL-10, Perforin/Granzyme… |
3. Sự khác biệt về chức năng và quá trình hoạt hóa tế bào
Tế bào NK và tế bào T gây độc có phương thức tiêu diệt tế bào đích tương tự nhau, sự khác biệt đến từ quá trình nhận biết và kích hoạt tín hiệu tiêu diệt của từng loại tế bào. Hoạt tính của các tế bào NK phụ thuộc rất nhiều vào sự cân bằng giữa các tín hiệu ức chế và tín hiệu hoạt hóa thông qua một loạt các thụ thể khác nhau trên bề mặt tế bào.
Các thụ thể trên bề mặt tế bào NK tham gia điều hòa hoạt động được chia làm 2 loại: (1) thụ thể hoạt hóa như NKG2D, NKp30, NKp44, NKp46...; (2) thụ thể ức chế như PD1, CD94/NKG2A, KIR-L... Cơ chế điều hòa hoạt động của các tế bào NK thông qua các thụ thể hoạt hóa và ức chế là rất phức tạp. Bình thường, các thụ thể ức chế của tế bào NK liên kết với các phân tử MHC lớp I biểu hiện trên hầu hết các tế bào của cơ thể, tín hiệu này làm bất hoạt các tế bào NK. Ở các tế bào bất thường, sự vắng mặt/thay đổi của phân tử MHC lớp I dẫn tới các thụ thể ức chế của tế bào NK mất liên kết với phối tử, tín hiệu kích hoạt chiếm ưu thế kích thích tế bào NK thực hiện chức năng tiêu diệt.
Cũng như tế bào NK, tế bào T gây độc được điều hòa bởi hệ miễn dịch rất chặt chẽ. Các tế bào trình diện kháng nguyên (tế bào đuôi gai, đại thực bào, tế bào B) bắt giữ các mảnh vỡ, đoạn peptide có nguồn gốc từ các tế bào bất thường để xử lý và trình diện sản phẩm là kháng nguyên lên các phân tử MHC. Kháng nguyên được trình diện trên phân tử MHC lớp I được tế bào T gây độc nhận diện và ghi nhớ, khi gặp các tế bào bất thường biểu hiện tế bào T gây độc nhanh chóng thực hiện chức năng “giết” của mình. Ngoài con đường điều hòa thông qua liên kết TCR với phân tử MHC lớp I, tế bào T gây độc cũng được kiểm soát bằng các thụ thể kích hoạt và ức chế. Một số các thụ thể của tế bào NK và tế bào T gây độc được tổng hợp tại bảng 2.
Bảng 2: Các thụ thể của tế bào NK và tế bào T gây độc
| Thụ thể | NK | T gây độc |
| Hoạt hóa | NKG2D, NKp30, NKp44, NKp46, NKp80, CD94/NKG2C, KIR-S, NKR-P1C, CD84, Ly9, act.Ly49, CRACC, 2B4… | TCR, CD27, CD28, CD69, CD95, OX40… |
| Ức chế | PD1, KIR-L, LILRB1, CD94/NKG2A, inh.Ly49, NKR-P1B, NKR-P1D, KLRG-1, LAIR-1… | CTLA-4, PD1, CD45, TNFR1, 2B4, LAIR-1, KLRG-1, PirB… |
| Chemokine | CCR2, CCR5, CCR7, CXCR1, CXCR3, CXCR4, CXCR6, CX3CR1, Chem23R, S1P5… | CCR1, CCR2, CCR5, CCR6, CXCR3, CXCR6, CX3CR1, S1PR… |
| Interleukine | IL-1R, IL-2R, IL-12R, IL-15R, IL-18R, IL-21R | IL-1R, IL-2R, IL-4R, IL-6R. |
| Liên kết | CD2, DNAM-1, β1 integrins, β2 integrins… | LFA1, CD54, CD29, Selectins, α4β7… |

Sự khác biệt về thụ thể liên kết, interleukine và chemokine cũng dẫn tới những chức năng khác nhau giữa hai dòng tế bào. Thụ thể interleukine quy định quá trình tăng sinh, phát triển, quá trình sản xuất cytokine, chất sinh miễn dịch của tế bào. Liên kết các interleukine với các thụ thể tương ứng kích hoạt các tế bào tổng hợp vật chất hữu cơ và phản ứng sinh hóa. Khác biệt về thụ thể interleukine giữa tế bào NK và tế bào T gây độc dẫn tới sự khác biệt về loại và mức độ sản xuất cytokine (bảng 1).
Trong đáp ứng miễn dịch chống lại tác nhân gây bệnh, một số loại tế bào miễn dịch như tế bào T hỗ trợ, đại thực bào... sản xuất chemokine để tổ chức, kêu gọi các tế bào miễn dịch khác tham gia. Các thụ thể chemokine khác nhau sẽ kết hợp với các chemokine tương ứng, quy định các tế bào khác nhau tham gia vào các phản ứng miễn dịch và mang vai trò chuyên biệt. Tế bào NK thể hiện khả năng đáp ứng nhanh trong vòng vài giờ sau khi nhận được tín hiệu (miễn dịch bẩm sinh) trong khi tế bào T gây độc cần từ vài ngày đến vài tuần để trải qua quá trình huấn luyện, trình diện trước khi tham gia đáp ứng (miễn dịch thích nghi).
Tế bào NK và tế bào T gây độc giữ những vai trò quan trọng trong hệ miễn dịch, chúng bù đắp hạn chế của nhau qua đó tăng cường khả năng tầm soát và loại bỏ mầm bệnh. Các thử nghiệm lâm sàng cho thấy điều trị ung thư bằng phương pháp kết hợp bằng tế bào NK và tế bào T gây độc mang lại hiệu quả cao hơn điều trị độc lập. Điều trị kết hợp mang lại hiệu quả đáp ứng nhanh của tế bào NK vừa có khả năng duy trì đáp ứng miễn dịch kéo dài của tế bào T gây độc.
Tài liệu tham khảo
- Eric Vivier et al.(2011). “Innate or Adaptive Immunity? The Example of Natural Killer Cells”, Science. 331(6013): 44–49. doi: 10.1126/science.1198687.
- Nomathamsanqa Resegofetse, Maimela,ShashaLiu,YiZhang.(2019). “Fates of CD8+ T cells in Tumor Microenvironment” .Comput Struct Biotechnol J. 17:1-13. doi: 10.1016/j.csbj.2018.11.004.
- Jillian Rosenberg and Jun Huang. (2018). “CD8+ T cells and NK cells: parallel and complementary soldiers of immunotherapy”. Curr Opin Chem Eng. 19:9-20. doi: 10.1016/j.coche.2017.11.006.
- Silvia A. Fuertes Marraco, Natalie J. Neubert, Grégory Verdeil and Daniel E. Speiser.(2015). “Inhibitory Receptors Beyond T Cell Exhaustion”. Front Immunol. 6: 310. doi: 10.3389/fimmu.2015.00310.
- Samuel C C Chiang et al. (2013). “Comparison of primary human cytotoxic T-cell and natural killer cell responses reveal similar molecular requirements for lytic granule exocytosis but differences in cytokine production”. Blood. 121 (8): 1345–1356. doi: 10.1182/blood-2012-07-442558.
- Stephen L.Nutt, Nicholas D.Huntington. (2019). “17-Cytotoxic T Lymphocytes and Natural Killer Cells”. Clinical Imunology (Fifth Edition). doi: 10.1016/B978-0-7020-6896-6.00017-X
- Raja Rajalingam. (2011). “Human diversity of killer cell immunoglobulin-like receptors and disease”. The Korean journal of hematology. 46(4):216-28. doi: 10.5045/kjh.2011.46.4.216.
Để đặt lịch khám tại viện, Quý khách vui lòng bấm số HOTLINE hoặc đặt lịch trực tiếp TẠI ĐÂY. Tải và đặt lịch khám tự động trên ứng dụng MyVinmec để quản lý, theo dõi lịch và đặt hẹn mọi lúc mọi nơi ngay trên ứng dụng.